赤塚結子(三重大学大学院医学系研究科),清水貴浩,岡田泰伸
細胞外及び細胞内の浸透圧変化に対応して自らの容積を一定に保とうとする働きは,動物細胞が生命を維持 する上で必要不可欠な機能であるが,最近ではこの容積調節の破綻が細胞死につながることが明らかとなっており,細胞がいかに自らの容積をセンスし対応する かという点に注目が集まっている。細胞が一旦膨張した状態から元の体積に戻る調節性容積減少 (regulatory volume decrease: RVD) の過程は,細胞内の蛋白質による情報伝達を介して,最終的には細胞内からのK+とCl-流出が駆動力となって細胞内の水が細胞外に流出することによって達成される。特にこの場合のCl-の通り道であるチャネルは細胞の容積上昇を感知して開口するために容積感受性Cl-チャネル(VSOR) と名づけられているが,このチャネル分子の実体が不明であるため,RVD分子のメカニズムにはわからない点も多い。
現在までに報告者は,VSORの調節蛋白質としてATP-binding cassette (ABC) 蛋白質スーパーファミリーに属するABCF2を同定しているが,今回の共同研究によって,ABCF2を大量発現させたHEK293T細胞ではVSOR電流 が著明に抑制されること,それに一致してRVDも著明にブロックされること,またsiRNAでABCF2の発現を抑制するとRVDは亢進することが明らか になった。さらに,ABCF2がアクチン結合蛋白質であるアクチニン-4と結合すること,その結合には両者のアミノ末端側領域が必要であること,またアク チニン-4を大量発現させたHEK293T細胞ではRVDが亢進し,siRNAでその発現を抑制するとRVDが抑制されることがわかった。つま り,ABCF2は直接的であるか間接的であるかは不明であるが,VSORを負に制御する調節因子であること,アクチニン-4はその抑制を解除する方向に働 くことが考えられた。この結果に基づき,ABCF2結合蛋白質を検索し,VSORの候補蛋白質の同定を試みている。
上田陽一,藤原広明,横山 徹(産業医科大学・医学部)
斎藤 健(産業医科大学・医学研究科)
バゾプレッシンは視床下部室傍核および視索上核に局在する大細胞性神経分泌ニューロンで産生され,下垂 体後葉に投射した軸索終末から血液中に分泌される。バゾプレッシン産生ニューロンには浸透圧感受性があり,血漿浸透圧の増加によってバゾプレッシン合成・ 分泌が促進される。我々は,バゾプレッシン産生ニューロンに特異的にGFPを発現するバゾプレッシン-GFPトランスジェニックラットを作製し,蛍光顕微 鏡下でGFP蛍光を指標に生細胞の状態でバゾプレッシンニューロンを容易に同定することを可能にした。本共同研究では,本トランスジェニックラットを用い て,バゾプレッシン産生ニューロンの浸透圧感受性についての詳細なメカニズムを解明することを目的としている。
我々は,これまで本ラットで5日間の高張食塩水飲水負荷により視床下部GFP遺伝子の発現が著明に増加することを明らかにした。今回,急性浸透圧刺激による視床下部GFP遺伝子の発現をc-fos遺伝子発現と比較検討した結果,血漿浸透圧とGFP遺伝子発現にc-fos遺 伝子発現ほどではないが有意な正の相関を認めた。さらに,本ラットの視索上核を含む脳スライス標本から急性単離したバゾプレッシン-GFPニューロンを用 い,細胞レベルでの浸透圧感受性を検討した。単離ニューロンは蛍光顕微鏡下で容易に同定することができ,ホールセルパッチクランプ法を用いた電気記録で は,バゾプレッシン産生ニューロンに特徴的な間欠型放電パターンを記録することができた。現在,マンニトールを用いた高浸透圧刺激による変化を解析中であ る。また,視索上核大細胞性ニューロンへの入力における浸透圧感受性についてホールセルパッチクランプ法を用いて検討し,興奮性入力は高浸透圧刺激により 有意に増加し,この反応はTRPVブロッカーであるルテニウムレッドによって抑制されることを見出した。また,抑制性入力は高浸透圧刺激によって影響を受 けないが,数時間にわたり高浸透圧状態にあると低浸透圧刺激に対して有意な増加反応を示すことを見出した。今後,バゾプレッシンニューロンの浸透圧感受性 に対するTRPVの関与,バゾプレッシンニューロンへのシナプス入力の浸透圧感受性において細胞内情報伝達系を含めた分子メカニズムについて検討する予定 である。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
関係論文
新谷隆史,野田昌晴(自然科学研究機構 基礎生物学研究所)
高橋信之,岡田泰伸
低浸透圧刺激等による細胞容積の増大で活性化されるイオンチャネルの中で,マキシ陰イオンチャネルは, グリア細胞などに発現し,シグナル分子として作用するグルタミン酸やATPの放出をもたらすことが知られている重要なイオンチャネルである。申請者らは, この低浸透圧刺激によるマキシ陰イオンチャネルの活性化が,受容体型タンパク質チロシン脱リン酸化酵素(受容体型PTP)阻害剤の添加により抑制されるこ とを見出した。そこで本申請共同研究では,細胞容積感受性イオンチャネル活性化制御における受容体型PTPの関与を解明することを目的とする。
まずパッチクランプ法を用いた電気生理学的解析により,PTP阻害剤の作用についての詳細な検討を行 い,PTP阻害剤の中で,vanadate,dephostatin,bromtetramisoleおよびチロシン脱リン酸化酵素阻害剤カクテルが,マ キシ陰イオンチャネルの低浸透圧刺激による活性化を阻害することが明らかとなった。
次に,野田らが作製した受容体型PTPであるPTP-zeta (z) ノックアウトマウスから線維芽細胞を調製して電気生理学的に検討したところ,野生型の細胞と比べて,マキシ陰イオンチャネルの低浸透圧刺激による活性化が有意に抑制されていることが判明した。
以上の結果は,マキシ陰イオンチャネルの低浸透圧刺激による活性化に,PTPが重要であること,特に受容体型PTPであるPTPzが関与している可能性が高いことを示唆する。今後,PTPzノックアウト繊維芽細胞に,PTPz発現ベクターを導入する回復実験などを行い,より詳細なマキシ陰イオンチャネル活性化機構を解析する予定である。
河田照雄,楠堂達也,後藤 剛,向井佐輝子,浅野 亘(京都大学大学院農学研究科)
岡田泰伸,高橋信之,井上 華
脂肪細胞は,脂肪を貯めることにより,その容積を約1~2万倍まで肥大化し,可逆的に維持しうる能力を 備えている。この脂肪細胞の肥大化は,肥満と密接に関連しており,さらに糖尿病や高血圧といった生活習慣病を引き起こす主要因である。そこで本研究では, 脂肪細胞が,自身でその発達度合いをどのようにモニターしているのか,その形態形成・容積維持・肥大化制御を行っているかを解明することを目的とする。
本共同研究で同定を試みる容積センサーは,成熟した脂肪細胞に特異的に発現していることが予想される。 そこで,まずDNAマイクロアレイ法によりマウス脂肪組織におけるイオンチャネルの発現解析を行った。その結果,機械刺激によっても活性化されることが報 告されている非選択性陽イオンチャネルTRPV2が,成熟脂肪細胞に特異的に発現していることが明らかとなった。そこでまず容積センサーの候補分子とし て,TRPV2に着目することとした。
分化した脂肪細胞でのTRPV2の機能解析を行うため,TRPV2を過剰発現させた小型脂肪細胞モデル 3T3-L1細胞を樹立した。この細胞に,TRPV2アゴニストである2-APBを添加すると,Fura-2によるカルシウムイメージング法により細胞内 カルシウムイオン濃度の上昇が観察された。さらに,TRPV2過剰発現細胞を用いてパッチクランプ実験を行ったところ,2-APBによりカルシウムイオン 電流が観察された。
次に,TRPV2の過剰発現が,3T3-L1細胞の脂肪細胞への分化にどのような影響を与えるかを検討 するため,上記のTRPV2過剰発現3T3-L1細胞に分化誘導処理を行い,分化誘導後に,各種分化マーカー遺伝子の発現定量などの脂肪細胞分化の評価を 行った。その結果,TRPV2過剰発現細胞では,複数の分化マーカー遺伝子の発現が有意に低下していた。また細胞質中の中性脂肪 (TG) の蓄積は,TRPV2過剰発現細胞で有意に抑制されていた。これら脂肪細胞の分化マーカー遺伝子の誘導やTG蓄積に関与することが知られている核内転写因 子の発現も,TRPV2の過剰発現により低下していた。以上の結果から,3T3-L1脂肪細胞分化に対して,TRPV2の過剰発現は抑制的に作用し,また その作用点は分化誘導・促進を担う核内転写因子の発現誘導よりも上流である可能性が考えられた。
加藤総夫(東京慈恵会医科大学・総合医科学研究センター・神経生理学研究室)
痛みの本質は不快な「情動的体験」であり,慢性痛の臨床医学的問題の核心は,原発症状消退後も持続する その苦痛や不快感,不安などの情動的側面にある。痛みの情動成分の成立に関与する神経回路として,Bernardらは脊髄後角浅層疼痛特異的ニューロンか ら上行し逆側脚傍核外側部 (PB) でシナプスを介した後,扁桃体中心核外側外包部 (CeLC) へと至るspino-limbic pathwayを同定した。CeLCは「nociceptive amygdala」とも呼ばれその78%のニューロンが侵害刺激によって興奮する。脊髄神経結紮神経因性疼痛モデルを作成し,allodynia応答を定 量評価した後,脳スライスを作成してPB-CeLC興奮性シナプス伝達を記録・解析した結果,CeLCにおけるシナプス伝達がallodynia成立の強 度に依存して増強される事実を見出し,今年度報告した (Ikeda et al.,Pain,127: 161-172,2007)。
このシナプス増強の形成機構の解明を目的として研究を進めた。CeLC興奮性シナプスの微細形態を神経 因性疼痛成立側と非成立側の比較検討のうえ解析した。細胞体近傍の非対称シナプスには,神経因性疼痛成立側と非成立側の間に著明な差が認められなかった。 今後PB由来の軸索の終末を同定して比較する必要がある。
一方,上記の電気生理学的実験で用いたスライス標本におけるPB-CeLC上行路のCeLC近傍での走行の順行性蛍光標識による同定を試みた。固定脳組織のPBにDiI結晶を装着し8週後,厚さ400mmの切片を作成したところ,CeA内側部にCeAに投射する神経束が観察され,刺激電極設置位置と一致していることが確認された。
さらに,神経因性疼痛モデル動物からCeAを含む脳ブロックを摘出し,digoxigenin標識したRNAプローブ(GluR1およびGluR2に対するsenseおよびantisense)を用いてin situ hybridizationを行ったところ,GluR1遺伝子の発現がシナプス伝達増強が生じている側のCeLCにおいて対側よりも増加している所見が得られた。
以上より,神経因性疼痛動物のPB-CeLCシナプスにおける機能的な伝達効率の変化は受容体発現レベルを含むシナプスの局所的かつ微細な変化によって生じている可能性が示された。
石橋仁(九州大学医学研究院)
桂林秀太郎(崇城大学薬学部)
賀数康弘(九州大学医学研究院)
鍋倉淳一(生理学研究所)
シナプスはシナプス前神経終末部,シナプス後細胞およびグリア細胞に囲まれており,シナプス周囲の細胞外スペースはそれほど広くない。シナプス伝達,特に高頻度のシナプス伝達の場合には,シナプス前神経終末部への Ca2+ 流入に加え,シナプス後細胞に Ca2+ が流入すると,シナプス周囲の細胞外 Ca2+ 濃度は急速に低下する。従って,細胞外からのCa2+ 流入に依存せずに,脱分極自体により神経終末部内でCa2+ ストアからのCa2+ 放出が起こる現象は,シナプス伝達とその修飾に重要な役割をしていると考えられる。本共同研究の目的は,神経終末部の脱分極がPLCの活性化を介して神経 伝達物質放出を増強するメカニズムを完全に解明し,さらにその生理学的な意義を明らかにすることにある。実験にはラット脊髄後角または海馬CA3領域より 機械的処理のみによって急性単離した神経細胞を用い,パッチクランプ法を適用することによって自発性抑制性シナプス後電流 (IPSC) を記録した。GABAまたはグリシン作動性IPSC を指標にして,実験を行った。細胞外 Ca2+-free 条件下,高K+ 溶液 (30mM) により神経終末部の脱分極刺激を行うと,自発性IPSCの頻度が著明に増加した。この IPSC の頻度増加は,高K+ 溶液を洗浄した後約10 分でコントロールのレベルに戻った。一方,細胞外の Na+ を除去した条件下では,高K+ 溶液自体のIPSC頻度増加作用に変化はないものの,洗浄後の回復がほとんど認められなかった。細胞外Na+ は Na+/Ca2+ 交換体を介した Ca2+ 排出に重要であることから,細胞外に Ca2+ がなくても,高K+ 刺激により細胞内 Ca2+ 放出が起こっていることが示唆された。実際,膜透過性の Ca2+ キレート剤である BAPTA-AM により,高K+ 刺激の応答が抑制された。高 K+ による神経終末部の脱分極によって,神経終末部内の Ca2+ 貯蔵部位から Ca2+ 放出が起こること,この機序に PLC の活性化が重要であることが明らかになった。
福田敦夫,熊田竜郎,古川智範(浜松医科大学)
鍋倉淳一,渡部美穂(生理学研究所)
発達および障害後の回路再編におけるCl-トランスポーターの関与を証明するため,以下の研究を行った。
ラットの限局性皮質形成異常モデルでは,poly microgyria類似の微小脳回形成過程の移動細胞において,取込型Cl-トランスポーターNKCC1の増加と排出型KCC2の減少による細胞内Cl- 濃度 ([Cl-]i) 上昇,その結果としてのGABAの抑制から興奮への変化が見られた。これらの変化は一種の脱分化で,5-6層の細胞は発生が早いため脱分化できず,脱分化 できた皮質板細胞のみがlesion部位に移動して微小脳回を形成したと考えられた。また,難治てんかん患者の摘出cortical dysplasia組織周囲の小型神経細胞ではKCC2が有意に減少しており,てんかん焦点におけるCl-ホメオスタシスの異常によるGABAの興奮性作用あるいは抑制作用の減弱が示唆された。paracrine的に放出されたGABAが脳の発達に重要であると考えられているが,内因性に大量に存在しGABAA受容体のアゴニストにもなり得るタウリンの影響は考慮されていなかった。そこで我々は母体のタウリン合成能を阻害したモデルを作成した。妊娠14日目に脳室帯の新生神経細胞特異的にHcRed遺伝子を導入した。その結果,タウリンがGABA以上にGABAA受容体の内因性アゴニストとして作用し,cortical plateにおけるradial細胞移動のstop signalとして働いている可能性を見出した。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
関係論文
西谷友重,若林繁夫(国立循環器病センター研究所)
鍋倉淳一(生理学研究所)
NCS-1 (Neuronal Ca2+ sensor -1) は,主に神経や心臓に発現しているCa2+結合タンパク質で,もともと神経のシナプス伝達に関わる因子として知られていた。私達は最近,“NCS-1が障害を受けた神経細胞においてその発現量が増加するサバイバル因子として働く”という全く新しい重要機能を見出した。そこで本研究では,1) NCS-1の神経細胞死抑制作用ならびに細胞機能回復作用をin vitro およびin vivo両方の系で確定すると共に,2) その詳細な作用機構を解明し,各種神経変性疾患における病態的意義を明らかにすることを目的とした。
1. 神経切断や各種ストレス下の神経細胞において,NCS-1の発現量が増加する。
2. その生理的意義はサバイバル促進作用。
3. NCS-1は,サバイバル作用をもつ神経栄養因子GDNFの下流に存在し,PI3K/Aktの経路を活性化することにより,そのサバイバル作用を仲介する。
4. 神経切断時においても神経が死滅しないのは内因性の抗アポトーシス機構によるものであるが,それにNCS-1が重要な役割を果たしている。
これらの発見は,NCS-1の全く新しい生理機能およびその分子機構を示したものであり,種々の神経変性疾患克服への応用が期待される。また,NCS-1は未成熟心筋にも高発現していることから,現在,心筋細胞における生理機能について検討中である。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
関係論文
片桐 秀樹(東北大学大学院医学系研究科再生治療開発分野)
石垣 泰(東北大学病院糖尿病代謝科)
山田 哲也(東北大学病院糖尿病代謝科)
箕越 靖彦
生活習慣病の基礎疾患である肥満症患者の爆発的増加が社会問題となっている。肥満症は,摂取エネルギー と消費エネルギーの差の増加によって発症するが,日々の食事量や活動量の変動がそのまま直接に体重の変化に反映されることはない。エネルギー摂取臓器,エ ネルギー貯蔵臓器,エネルギー消費臓器が密接に連携を取り合い,情報を共有することによって体重の恒常性を維持しているからである。本研究では,糖・脂質 代謝の変化を視床下部がどのように感知し,求心性神経,交感神経によってどう調節しているかを明らかにすることを目的に研究を行った。さらに,その破綻と 考えられる肥満・糖尿病やメタボリックシンドロームの発症機序の解明および治療法開発につなげることを目的とした。
肥満・糖尿病・高脂血症のマウスモデルを用い,アデノウィルスを用いた後天的遺伝子導入の手法等によ る,エネルギー代謝調節における末梢組織と中枢との情報のやりとりについて検討した。その結果,脂肪組織からの求心性神経シグナルが食欲の調節に関与して いること,肝臓からの求心性神経シグナルがエネルギー代謝情報を中枢に伝え,交感神経遠心路の活動の変化を介して全身のエネルギー代謝の調節が行われてい ることを見出した。また,末梢組織における脂肪の取り込みを抑えることで,中枢におけるエネルギー摂取や消費が変化すること,さらに,交感神経遠心路の活 性化が,脂肪組織におけるアディポサイトカインの一つアディポネクチンの発現に影響を与えることを見出した。これらから,ホルモン因子と自律神経シグナル は互いに協調して全身の代謝を調節し,さらに,中枢神経系がその統御を行う仕組みが示唆される。現在,中枢神経系の局所への遺伝子導入や破壊・切断等の手 技を用いて,検討を進めている。上記,末梢組織での代謝変化誘導の手法を組み合わせて,これらの末梢組織からの代謝情報を中枢が受け取りプロセスしていく 機構につき,生理学研究所生殖・内分泌発達機構研究部門 箕越靖彦教授の研究室との共同研究をさらに発展させていきたいと考えている。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
門脇 孝(東京大学大学院医学系研究科糖尿病代謝内科)
窪田 直人(東京大学大学院医学系研究科糖尿病代謝内科)
窪田 哲也(東京大学大学院医学系研究科糖尿病代謝内科)
伊藤 晋介(東京大学大学院医学系研究科糖尿病代謝内科)
箕越 靖彦
アディポネクチンは,レプチンとともに脂肪細胞から分泌されるアディポカインである。レプチンは中枢で は生体内エネルギーセンサーである視床下部でAMPK活性を低下させることにより摂食を抑制し,末梢では骨格筋におけるAMPK活性を上昇させ脂肪酸酸化 を促進させる。一方アディポネクチンも肝臓,骨格筋においてAMPK活性を上昇させ脂肪酸酸化を促進し,インスリン感受性ホルモンとして作用することが明 らかとなっているが,中枢におけるその役割はまだ不明である。そこで本研究では,アディポネクチンが視床下部においてどのような調節作用を営んでいるかを 調べた。
我々は,まずはじめに,視床下部におけるアディポネクチン受容体の発現を調べた。2つのアディポネクチ ン受容体,AdipoR1/AdipoR2はいずれも視床下部において発現が認められ,その程度は肝臓での発現量に匹敵した。さらに,AdipoR1 /AdipoR2の発現はいずれもレプチン受容体が強発現している視床下部の特に弓状核の部分に強く認められた。次に我々は髄液中にアディポネクチンが存 在するかどうかについて調べた。髄液中のアディポネクチン濃度は血中の約1/5000程度存在した。また,血清と髄液のアディポネクチンの分画について検 討したところ,血清では高分子量が多く検出されたが,髄液では高分子量はわずかで,主に中分子量が多く検出され,中枢では主に中分子量のアディポネクチン が作用すると考えられた。さらに摂食とアディポネクチンの関連について検討したところ,血中のアディポネクチン濃度と視床下部におけるAdipoR1の発 現は絶食時に上昇し,逆に摂食後低下することが明らかとなった。これに対してAdipoR2 の発現は絶食,摂食後で有意な変化は認められなかった。次に外来性にアディポネクチンを脳室内に投与した。その結果,摂食後に低下した視床下部のAMPK 活性が,アディポネクチン投与により,絶食時とほぼ同程度まで上昇することを見出した。また,AMPK活性と一致して,摂食量も増加した。以上のことよ り,アディポネクチンは中枢,特に視床下部において摂食さらには個体のエネルギー調節に重要な役割を果す可能性が示唆される。これらの結果は,現在,論文 に投稿中である。
益崎 裕章(京都大学大学院医学系研究科内科学講座内分泌代謝内科)
田中 智洋(京都大学大学院医学系研究科内科学講座内分泌代謝内科)
箕越 靖彦
レプチンは視床下部・交感神経系を介して骨格筋AMPキナーゼを活性化し,糖脂質代謝を亢進する。我々 は最近,高脂肪食性肥満の病態においてはレプチンによる骨格筋AMPキナーゼ活性化が減弱することを示しメタボリックシンドローム治療におけるレプチン抵 抗性解除の重要性を明らかにした (Tanaka T et al. Diabetes 54:2365,2005)。本研究ではレプチン抵抗性の分子メカニズムを探索し,骨格筋糖脂質代謝調節における中枢メラノコルチン系の意義を明らかにす る目的で,種々のモデル動物に対するメラノコルチン受容体アゴニスト,アンタゴニストの中枢投与を行い,骨格筋AMPK,下流のacetyl CoA carboxylase (ACC) のリン酸化を検討した。
マウス脳室内カニューラ,皮下カニューラを留置・馴化させ,カニューラより以下に述べる薬剤を脳室内投 与(一日2回,5日間)し,皮下カニューラからの過剰量抱水クロラール投与にて麻酔後,骨格筋のサンプリングを実施した。この方法は実験上の様々なストレ スや飼育環境によって容易に変動する骨格筋AMPキナーゼ活性を極めて安定的かつ再現性をもって評価することが出来る方法であり,生理学研究所の箕越靖彦 教授の御指導によって確立した。骨格筋AMPキナーゼ活性化の評価には,リン酸化AMPキナーゼ抗体,AMPキナーゼの直下流に位置するACC(アセチル CoAカルボキシラーゼ)リン酸化抗体,サムスペプチドを用いた酵素活性の測定と骨格筋中性脂質含量測定を利用した。
マウスの脳室内にメラノコルチン受容体アゴニスト(MT-II) を投与すると,骨格筋AMPKおよびACCのリン酸化が顕著に亢進した。レプチンによる骨格筋AMPKおよびACCのリン酸化の増加は,メラノコルチン受 容体アンタゴニスト (SHU9119) の脳室内共投与,あるいは内因性メラノコルチン拮抗物質,agouti蛋白を視床下部で異所性に高発現する遺伝性肥満KKAyマウスにおいて明らかに減弱 した。これらの実験により,骨格筋AMPKの活性化の減弱がレプチン抵抗性の程度とよく相関すること,さらに,メラノコルチンアゴニストが先天的,後天的 に誘導されたレプチン抵抗性の状態にも効果を発揮することが明らかとなった。以上の実験結果は,現在,論文に投稿中である。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
塩田清二(昭和大学医学部第1解剖学教室)
舟橋久幸(昭和大学医学部第1解剖学教室)
影山晴秋(昭和大学医学部第1解剖学教室)
竹ノ谷文子(星薬科大学薬学部体育学研究室)
箕越 靖彦
摂食調節や生体のエネルギーの恒常性を司るのが視床下部の化学受容ニューロンであり,栄養状態で変動する血中グルコース,遊離脂肪酸やホルモンなどの末梢からの情報をこのニューロンは感知している。しかしオレキシン,ガラニン様ペプチド (GALP) やグレリンなどの新規Gタンパク質共役型レセプター(GPCR) リガンドの発見により,摂食調節研究は大きな転換点を迎えている。そこで摂食行動を結ぶ神経機構を機能形態学的に解析することを目的として研究を行った。
満腹中枢として機能する視床下部腹内側核 (VMH) にはグルコース受容ニューロンが存在することが知られているが,どのような神経ペプチドを産生するニューロンであるかは未だ不明である。外側視床下部にあ るオレキシン含有ニューロンの軸索がVMHに豊富にあることから,VMHニューロンのマーカーであるSF-1転写因子と2重免疫染色を行い,オレキシン ニューロンとVMHニューロンとの神経相関をしらべた。オレキシン免疫陽性ニューロンの軸索はVMHおよび第3脳室周囲部に分布していた。またSF-1免 疫陽性細胞はVMHに限局して存在していることを確認した。オレキシン免疫陽性ニューロンの軸索はSF-1免疫陽性ニューロンへ投射していた。その投射は VMH内側よりも外側で多く観察された。この結果から,オレキシンはVMHを介して,摂食調節を行っていることが示唆された。今後はこの投射が生理学的に どのような意義を持っているのかを検討して行く予定である。
GALPは摂食調節ペプチドとして知られているが,我々や他の研究グループの報告によりエネルギー代謝 を亢進することが明らかとなってきた。しかしながら,末梢組織でのエネルギー代謝調節は不明である。そこでGALPを脳室内投与した時の末梢組織でのグル コース取り込み量を2-デオキシグルコース (2-DG) の取り込み量で測定した。その結果,GALP投与で骨格筋の腓腹筋,ヒラメ筋,長指伸筋で2-DGの取り込み量を有意に増大させたが,褐色脂肪組織や白色 脂肪組織など他の組織では有意な変化はなかった。これらの結果から,GALPは骨格筋のグルコースの取り込みを増大させることが明らかとなったので,今後 中枢から骨格筋でのエネルギー代謝の情報経路を神経解剖学的さらには組織レベルで検討して行く予定である。
中里 雅光(宮崎大学医学部内科学講座神経呼吸内分泌代謝学分野)
山口 秀樹(宮崎大学医学部内科学講座神経呼吸内分泌代謝学分野)
上野 浩晶(宮崎大学医学部内科学講座神経呼吸内分泌代謝学分野)
伊達 紫(宮崎大学フロンティア科学実験総合センター)
十枝内 厚次(宮崎大学医学部内科学講座神経呼吸内分泌代謝学分野)
箕越 靖彦
摂食とエネルギー代謝調節は,中枢と末梢で産生される物質の複雑な相互関係により,巧妙に調節されてい る。視床下部は,エネルギー代謝調節の中枢として機能しており,どのような分子が働いているかを明らかにすることは中枢性代謝調節を理解する上で,重要で ある。われわれは,新規摂食調節物質の探索を行い,グレリン,神経ペプチドW,ニューロメジンU,アスビオシンなどの新規ペプチドを発見するとともに,消 化管で産生される摂食調節ペプチドの多くが,迷走神経求心路を介して,末梢情報を中枢に伝達することを明らかにしてきた。本研究は,脳幹の孤束核に伝達さ れた末梢情報がどのように視床下部に伝達されるか,また視床下部における神経間の分子情報伝達機構を明らかにすることで,摂食調節系の分子機構を解明する ことを目的とした。
われわれはグレリン,コレシストキニン,ペプチドYYの摂食調節シグナルが迷走神経を介して,視床下部 に伝達されることを明らかにしてきた。本年度は,さらに末梢におけるインスリンの変動が肝臓によって受容され,迷走神経を介して,中枢に伝達されることを 明らかにした。また,本研究において末梢におけるグレリンの摂食亢進作用は,孤束核でノルアドレナリン神経を活性化し,投射先である視床下部弓状核のノル アドレナリンa1もしくはb2受容体を 介して摂食亢進に機能することを見出した。さらに,視床下部において,中枢での生理作用が不明であった脱アシル化グレリンが,摂食亢進に機能し,グレリン システムは総合的に摂食亢進に作用していることを見出した。また,加齢に伴い内因性のグレリン分泌は減少するが,グレリン投与による摂食亢進作用は,世代 に関係なく維持されており,グレリン補充が生体機能維持に有効であることを明らかにした。これらグレリンの摂食亢進機序に加えて,中枢投与において摂食抑 制に機能する神経ペプチドWも胃で産生されており,絶食による分泌抑制と再摂食による分泌亢進を見出した。現在,末梢で唯一摂食亢進に機能するグレリンを 摂食亢進シグナルのバイオマーカーとして利用することを検討している。これらの実験結果は,末梢と中枢で複雑なネットワークを形成している摂食調節機構の 解明に貢献すると考えている。
八木健,平林敬浩,金子涼輔(大阪大学大学院・生命機能研究科)
平林真澄(生理学研究所・遺伝子改変動物作製室)
クラスター型プロトカドヘリン分子群であるCNR(Cadherin-relatedneuronalreceptor) /プロトカドヘリンaファミリーはマウスでは14分子種が存在しており,いずれの分 子種も主に中枢神経で発現が認められている。その遺伝子構造は各分子種ごとに異なる多様化したエクソンが縦列した可変領域と共通にスプライシングされる3 つのエクソンからなる共通領域で構成され,各CNR/Pcdha分子種はひとつの可変領域エクソンと共通領域エクソンがスプライシングされ発現している。各分子種の発現様式を単一プルキンエ細胞レベルで解析した結果,一つのプルキンエ細胞では CNR/Pcdhaは複数の分子種を発現し,その分子種の組み合わせは個々のプルキ ンエ細胞ごとに異なっていた。また,発現している各分子種について染色体由来を調べると,片方の染色体のみに由来するものが多数であったことから,同分子 群はニューロンの個性(多様性)を担う分子であることが予想される。
本研究ではCNR/Pcdha分子群の中で最も発現量が多く,単一プルキンエ細胞での発現解析においてほぼ全ての細胞において発現していたCNRc2アイソフォームに着目し,種々のトランスジェニックマウス作製を行った。
まず,同分子の発現様式を詳細に解析することを目的とし,CNRc2プロモータの制御下で蛍光タンパク質EGFPを発現する外来遺伝子を導入したTgマウスを作製した。このTgマウスを組織学的に解析したところプルキンエ細胞の他に,嗅球,海馬などCNR/Pcdha分子群が発現している組織において蛍光が観察された。また,このTgマウスの脳から採取した神経細胞をEGFPの蛍光を指標にセルソーターで分取しCNR/Pcdha分 子群を発現している細胞のみを単離することを試みている。さらに動物個体での分子機能解析を行うためにCNRc2アイソフォームをCre酵素の発現により コンディショナルに過剰発現するTgマウスを作製した。現在,このTgマウスについて神経回路形成における異常などの組織学的解析を進めている。
【追加情報】(調査月2007年8月、記入月2008年6月)
関係論文
鈴木敦詞,安田啓子,関口佐保子(藤田保健衛生大学・内分泌代謝内科)
長尾静子(藤田保健衛生大学・疾患モデル教育研究センター)
平林真澄(生理学研究所・遺伝子改変動物作製室)
老化に伴う変化では骨組織より軟部組織へのカルシウムの移行がその一因と想定されている。細胞外基質石 灰化の中核をなす基質小胞でのリン酸取り込みを担う細胞膜Ⅲ型Na依存性リン酸輸送担体Pit-1遺伝子を過剰発現するトランスジェニック (Pit-1/Tg) ラットを共同研究にて作製したが,このPit-1/Tgラットは腎臓での糸球体障害を惹起し,生後8週目頃より巣状の糸球体障害が明らかとなり,低アルブ ミン血症,蛋白尿,高脂血症というネフローゼ症候群パターンを示した。このPit-1の過剰発現によるネフローゼ症候群の発症には腎糸球体での上皮細胞に 対する細胞外リンによる負荷が関与することが想定されたため,経時的にその変化を検討するとともに,invivoで骨代謝マーカー,カルシウム・リン代謝 について検討した。糸球体の変化は,出生直後から糸球体成熟時期に至る時期から基底膜の肥厚がはじまり,最終的には上皮細胞足突起構造の消失に至った。終 末期には糸球体の一部では半月体形成も認められ,腎硬化症を示唆する所見であった。InvivoでのPit-1Tgにおける血清リン濃度の上昇は TmP/GFRの上昇をともない,この変化は糸球体での変化よりも,近位尿細管血管腔側でのPit-1活性の上昇を反映すると考えられた。また雌Pit- 1Tgラットでは軽度の低カルシウム血症に起因する副甲状腺機能亢進症が認められたが,ビタミンD濃度に関しては何ら影響を認めなかった。新規リン利尿因 子であるfibroblastgrowthfactor23 (FGF23) は血清リン濃度と負の相関を示し,FGF23が少なくとも近位尿細管血管腔側のリン輸送の制御に関して,主な調節因子である可能性は低いと考えられた。
本間光一,山下真二(帝京大学)
黒川竜紀
【目的】本研究課題では,鳥類(ニワトリ)の胚発生および脳機能におけるVSPの役割を生化学的,生理学的に解析することにより,その生理機能を明らかにすることを目的とする。具体的には,1. VSPの胚発生時と孵化後における遺伝子発現の変動と組織局在。2. 胚発生時におけるVSP遺伝子の過剰発現系と遺伝子抑圧系を用いた必要性の証明。3. 孵化直後に見られる学習記憶(親子関係の刻印付け)における遺伝子発現変化。4. VSPによる細胞内情報伝達メカニズムの生化学的,生理学的解析。の以上4点について明らかにしてゆく。
【途中経過】電位センサー蛋白VSPは最初ホヤのゲノムから同定されたが,脊索動物に幅広く存在し,各動 物種での分子機能,生理機能を解析することにより,膜電位シグナル伝達におけるVSPの役割が解明できると期待される。脊椎動物の中でニワトリは,初期発 生の解析が進んでいるとともに,刷り込みなどの動物行動の優れた実験系である。神経系でのVSPの役割を理解するため,トリVSPのcDNAを同定し,発 現実験によりその分子機能を同定するとともに,ニワトリ神経系でのVSPの遺伝子発現を調べた。
その結果,トリVSP(以下Gg-VSP)は,tsA201細胞においてゲート電流を発現し,電位感知 機能があることが明らかになった。さらにGg-VSPの細胞内ドメインをGST融合蛋白として大腸菌に合成させ,マラカイトグリーンアッセイによりイノシ トールリン脂質の脱リン酸化能を調べたところ,Ci-VSPやゼブラフィッシュVSPと同様な基質特異性を示した。これらのことから,基本的にGg- VSPはCi-VSPとほぼ同様な分子機能を有すると考えられた。さらに,神経系での遺伝子発現をinsituhybridization法により検討し た結果,大脳皮質の大きめの細胞と小脳プルキンエ細胞に発現が認められた。とくに小脳プルキンエ細胞での発現は,キメラ状のパターンを示し,活動依存的な 発現により誘導される可能性が示唆された。さらに,蛋白レベルでの発現様式を明らかにするため,Gg-VSPの細胞内領域とGSTの融合蛋白を抗原として 用いてウサギに免疫し,ポリクローナル抗体を作成した。これを用いて発現様式を解析したところ,プルキンエ細胞での著明な発現が検出された。大脳皮質での 発現は明確ではなかった。
これらの結果から,トリの神経系ではVSPは小脳機能と関連していることが示唆された。今後,アフィニティー精製した抗体を用いて上記の知見を確認するとともに,培養細胞などの系を用いてプルキンエ細胞でのVSPの役割を明らかにする実験を行う予定である。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
関係論文
高橋 弘樹,山田 成宏,堀田 耕司,小笠原 道生,岡戸 晴生,
西野 敦雄,木下 典行,稲葉 一男,岡村 康司
神経発生過程における細胞間相互作用には生物種間で高度に保存された膜タンパク群の分子機能が重要であ る。しかし,これら膜タンパク質群の分子機能は遺伝子の点と点の繋がりとしては解明されているがダイナミックな時系列としての理解には程遠い。本研究で は,近年ゲノム情報が整備されるとともに単一細胞レベルでの個体発生が記述された原索動物ホヤ胚やEST情報が整備されたアフリカツメガエル胚を用い,神 経発生関連膜タンパク質とくにNotchシグナルや膜電位センサー分子のダイナミックな分子機能を個体まるごとのシステムで時系列的に解析を進めることを 目的とした。
1) 神経形成における脊索の役割
脊索動物の発生過程において,脊索は体軸伸長において働くのみならず,神経誘導や神経管形成過程におい ても重要な役割を果たしていると考えられているが,その分子メカニズムについては明らかにされていない点が多い。これまでに,我々はホヤのCi- fibrn (Ci-Fibrinogen-like)のmRNAは脊索細胞のみに特異的に発現することを脊索動物で初めて明らかにしている。興味深いことにCi- fibrnタンパク質の局在をCi-fibrn抗体とGFP融合タンパク質を用いて調べたところ,脊索細胞および脊索細胞外の表皮感覚細胞および中枢神経 細胞に沿った繊維状の構造に局在することが明らかになった(図1)。
2) 神経-脊索相互作用を担う膜タンパク質
ショウジョウバエのScabrousは遺伝学的な解析からNotchと相互作用することが示唆されてい る。そこで,NotchとScabrouのホモログであるCi-fibrnの関係を解析すると,NotchシグナルによってCi-fibrnタンパク質の 局在そのものが変化することが明らかになった。また,培養細胞を用いた免疫沈降実験からNotchの細胞外ドメインとCi-fibrnのC末端部分が結合 することが示された。さらに,Notchシグナルを阻害すると同時にCi-fibrnの変異体を発現させると幼生期では,頭部において神経細胞の分化異 常,尾部において神経軸索の走行異常が観察された。このことから,Ci-NotchとCi-fibrnは,神経細胞分化・形成において協調的に働いている ことが示唆されており,機能解析を進めている。
発表論文
Hotta,K., Yamada,S., Ueno, N., Satoh, N. & Takahashi, H. Brachyury-downstream notochord genes and convergent extension in Ciona intestinalis embryos.Dev. Growth Differ. 49, in press (2007).
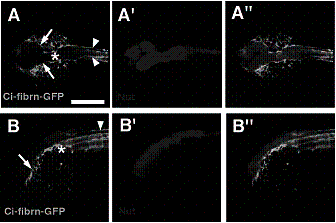
図1. カタユウレイボヤの幼生期におけるCi-fibrnの局在 (A)頭部脊側から見たCi-fibrnの局在 (B)頭部側面から見たCi-fibrnの局在。 CNSマーカーであるCi-Nut:RFPとの二重染色像。*: 脊索の最前位 矢印:頭部脊側のCi-fibrnの発現 矢尻:尾部脊側のCi-fibrnの発現
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
関係論文
宮脇敦史,筒井秀和,水野秀明,片山博幸,村田喜理
電位センサーはポア領域と並んで電位依存性チャネルの重要なモジュール構造であり,3次元結晶構造が解 かれたことを契機に,ここ数年分子動作原理を巡って熱い論争が続いている。最近尾索類のゲノム情報から電位依存性チャネルの電位センサーモジュールと酵素 モジュールを合わせもつ新規分子が同定され,電位センサータンパクの動作原理の解明とそれに基づく応用のための新しい材料が提供された。本研究では新規電 位センサー蛋白において膜電位変化による分子内情報伝達機構を明らかにするとともに,モジュールの変異導入や他の分子との組換えにより新規機能の創成を目 指した。
電位センサー蛋白VSPとVSOPの膜貫通ドメインを蛍光タンパクに融合させたコンストラクトを数種類 作成し,発現系細胞に発現させ,フォトマルチプライヤーを用いて膜電位依存的な蛍光強度の変化が生じるかを検討した。数種類の例で,蛍光強度の変化を検出 することができた。電位センサードメインにさまざまな変異を導入し,時間分解能を上げるとともに,蛍光強度の変化が生じる膜電位範囲を生理的な範囲 (-60mVから+20mV)にシフトさせることを行った。
また,PTEN (phosphataseandtensinhomologdeletedonchromosome10) は,膜貫通ドメインを含まないが,VSPの細胞内領域と高い相同性を示す。VSPにおける膜電位依存的な酵素活性の制御機構を明らかにする試みとして, PTENにVSPの電位センサーを融合させ,酵素活性を膜電位依存的に制御できるかを検討しようとしている。そのための準備として,PTENの活性中心の アミノ酸配列をVSP型に変更し,PtdIns(4,5)P2を基質とする脱リン酸化能を生じさせる実験を試みた。AlanineをGlycineに変更 したPTENをGST融合蛋白として大腸菌に合成させ,マラカイトグリーンアッセイを行ったところ,PTEN本来の基質である PtdIns(3,4,5)P3だけでなく,PtdIns(4,5)P2も脱リン酸化されることを見出した。今後VSPの膜貫通ドメインとの融合蛋白を作 成し,ツメガエル卵母細胞の発現系を用いてVSP-PTENキメラから膜電位依存的な酵素活性が検出されるかどうかを検討する予定である。
斎藤成也,隅山健太,増山和花,西野敦雄
【目的】バイオインフォマティクスの手法を用いてVSPなどのイオンチャネル関連分子について脊椎動物祖先型分子を推定し,その機能を発現実験により解析するとともに,脊椎動物の進化過程での機能改変のためゲノム的動態を明らかにする。
【結果】
(1) 系統樹解析
電位センサー蛋白VSPは,脊索動物に幅広く存在し,昨年度の系統樹解析により哺乳類において進化速度 が速いことを見出した。今年度は哺乳類と鳥類の中間であるオポッサムおよび棘皮動物であるウニのVSPの遺伝情報を用いて系統樹を作成し直すともに,酵素 ドメインの機能解析を行った。その結果,動物進化の系統樹と同様にオポッサムVSPは哺乳類と鳥類のVSPの間に位置し,前回得られた哺乳類で進化速度が 速いという知見を支持した(図参照)。また,ウニVSPはもっとも基部に位置し,脊索動物のVSPの起源に関連が深いことが推察された。
(2) 生化学実験による酵素活性の比較
マウスVSPの細胞内領域とGSTの融合蛋白を蛋白精製し,マラカイトグリーンアッセイ法によって,基 質特異性を調べた。マウスVSPはPtdIns(4,5)P2を脱リン酸化することを見出し,Ci-VSP,ゼブラフィッシュVSPと同様な酵素特性を示 すことが明らかになった。更に,Xenopus VSPについても同様な解析を行い,他のVSPと同様にPtdIns(4,5)P2を脱リン酸化する活性があることを明らかにした。これらVSPが共通に PtdIns(4,5)P2を脱リン酸化する原因を明らかにするため,VSPと相同であるがPtdIns(4,5)P2を脱リン酸化できないPTENとの アミノ酸配列の比較を行ったところ,活性中心のアラニンがVSPでは共通にグリシンになっていることに気づいた。このグリシンをアラニンに変更する と,PtdIns(4,5)P2への酵素活性が失われることが,マラカイトグリーンアッセイおよびTLC (Thin layer chromatography) による解析で,明らかになった。
(3) ウニVSPの分子特性を明らかにするため,発現系細胞を用いて電気生理学的計測を行った。tsA201細胞ではゲート電流は見られなかったが,ツメガエル 卵母細胞においてはOFF電流が計測された。GIRK2を用いて電位依存性PtdIns(4,5)P2酵素活性を調べたところ,弱いながら,電位感受性が 検出された。いまのところ,発現量に問題があると考えられるので,Ci-VSPと同程度の電位感受性があるか否かは明確ではないが,哺乳類以外のVSPは ウニからトリまで電位感知機能が備わっていると考えられ,哺乳類で生理機能が特殊化された可能性が示唆された。今後入手が困難であることが予想されるが, オポッサムのVSPのcDNAを用いて電位センサー機能を解析したい。
以上のことから,(ウニについてはまだこれからであるが)動物種を超えてVSPの酵素特性は共通である こと,哺乳類においては遺伝子配列の進化速度が加速していること,電位センサー特性は動物種によって大きく異なることから,VSPは進化の過程で電位感知 機能は変えたものの酵素活性の特性は変化させず,進化の過程で共通の細胞内シグナルを媒介することになったと考えられる。
永井 健治(北海道大学電子科学研究所・教授,提案代表者)
東島 眞一(自然科学研究機構・岡崎統合バイオサイエンスセンター)
提案代表者らは,遺伝学的にコードされたカルシウムインディケーターであるcameleonを従来より 高感度にチューンすることに成功している。本研究では,その新世代cameleonであるYC3.6および YC2.6を,イメージングに適した生物ゼブラフィッシュに適用して,神経発生過程におけるカルシウムシグナルの役割を調べることを目的とした。まず,カ ルシウムへのアフィニティが低い方のYC3.60を,体全体で発現を促すプロモーターであるリーク型のhsp70bプロモーターのもとにつないだコンスト ラクトによりトランスジェニックフィッシュを作製した。アフィニティが低い方をまず用いた理由は,シグナルが得られるならば,そちらの方がよりカルシウム の濃度変化のタイムコースを忠実にモニターしてくれることが期待されたためである。得られたトランスジェニック胚を用い,1日胚でみられる自発的神経活動 (1秒に1度ほどの頻度で,体全体を一方向へ屈曲させる自発的運動)に伴うカルシウムシグナルが得られるかどうか検討したところ,期待するようなシグナル は得られなかった。カルシウムへの感受性が低い方のインディケーターを用いたのがネガティブな結果の原因であると考え,感受性が高い方のインディケーター YC2.60を用い,hsp70bプロモーターによるトランスジェニックフィッシュを作製した。現在,このトランスジェニックフィッシュを用いてカルシウ ムイメージングをおこなっている段階である。
宇理須恒雄,手老龍吾(分子科学研究所)
小中信典(徳島大学工学部)
富永真琴(生理学研究所・岡崎統合バイオサイエンスセンター)
分子科学・材料科学分野のシリコン表面ナノ制御技術およびアレイ構造形成技術と生命科学分野の膜タンパ ク発現・精製技術とを融合し,新たにシリコン基板上への膜タンパク/脂質二重膜の集積技術を開発するとともに,これを発展させて,シリコン電子集積回路と 統合した,新規バイオ分子センサーを開発することを目的とする。さらに,単一チャンネル単一イオン計測など新たな膜タンパク電気生理特性の新規計測法や, ゲノム創薬用大規模スクリーニング応用素子の開発基盤を確立する。絶縁特性が良い事で知られているSOI (Si on Insulator) 構造のシリコン基板をもちい,これにさらに酸化膜を形成することで,テフロン並の低雑音基板を実現できることを理論的示し,実際に,グラミシジン/DfPCの系でテフロン基板なみの低雑音で単一イオンチャンネル電流の観測に成功した。世界にも例の無い,体内(脳内)埋め込みやマイクロ流体回路埋め込みを目指した超小型プレーナー型パッチクランプバイオセンサーの製作を目指して,開発を進めた。厚さ600mm のSOI基板に直径1mm 前後の微細貫通孔を形成する技術を開発した。収束イオンビームによる方法とプラヅマエッチングによる方法の二通りを開発したが,今のところ,収束イオン ビーム法のほうがシール抵抗で良好な結果が得られている。ついで,この微細貫通孔にHEK293細胞を設置し,ホールセルモードを形成した後,カプサイシ ン刺激によるチャンネル電流の観測に成功した。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
水村和枝,片野坂公明,矢島弘毅,申正樹(名古屋大学環境医学研究所)
富永真琴(生理学研究所・岡崎統合バイオサイエンスセンター)
現在までに明らかになっている9つの温度感受性TRPチャネルのうち5つは体温近傍の温かい温度で活性 化する。このうち,TRPV3,TRPV4は表皮ケラチノサイトに強く発現することが知られている。TRPV3,TRPV4は温度情報を電気信号に変換す る温度センサーとして機能するが,温度感覚が感覚神経から中枢に伝達されて初めて生じることは,ケラチノサイトで感知された温度情報が何らかの形で感覚神 経に伝達されることを示唆する。これまでの形態学的な研究から,ケラチノサイトと感覚神経の間にはシナプスのような構造は存在しないことが知られている。 新生仔マウスの表皮ケラチノサイトと後根神経節細胞の共培養系を確立した。ケラチノサイトはCa2+要求性が小さく,Ca2+を必要とする感覚神経細胞との共培養は困難をきわめたが,最適条件を見いだした。その共培養の細胞に温度刺激を加えて,細胞内Ca2+濃度の変化を観察した。放出される物質が洗い流されないようにチェンバー溶液の流れを止めて,チェンバー自身を加熱した。40度までの温度刺激によって両細胞で細胞内Ca2+濃度増加が観察された。しかし,ケラチノサイトに比べて神経細胞で細胞内Ca2+濃 度増加の遅れがみられ,平均して1.2秒の遅れであった。この遅れは,ケラチノサイトから感覚神経細胞に情報が伝達されるという仮説を支持する結果であ る。ケラチノサイトからは種々の刺激に応じてATPを放出することが知られている。そこで,ATP受容体阻害剤であるPPADS (100 mM) もしくはsuramin (100 mM) で前処理したところ,感覚神経細胞での細胞内Ca2+濃度増加のみが特異的に阻害された。この結果から,温度刺激によってケラチノサイトからATPが放出されて感覚神経に発現するATP受容体に作用することが強く示唆された。
門脇辰彦,辻内誠也(名古屋大学大学院生命農学研究科)
富永真琴(生理学研究所・岡崎統合バイオサイエンスセンター)
2003年に侵害性冷刺激受容体として遺伝子クローニングされたTRPA1は,その後複数の侵害刺激 (わさび,マスタードオイル,シナモンなど)によって活性化される侵害刺激受容の中心的分子として注目されている。TRPAファミリーとTRPMファミ リーに属するミツバチTRPチャネル6つをクローニングして哺乳類expression vectorに入れたコンストラクトを作成した。その6つのミツバチTRPチャネルをHEK293細胞に強制発現させて,Ca2+イ メージング法を用いて温度感受性を検討した。ミツバチの体温はそれほど高くないので,HEK293細胞は33度で培養した。事実,37度で培養した時には 温度刺激による反応がみられなかったTRPチャネルが33度で培養すると温度刺激に対して大きな反応がみられることがあった。検討した6つのTRPチャネ ルのうちTRPAファミリーに属する1つのチャネルを発現させたHEK293細胞に置いて40度までの温度刺激に対して細胞内Ca2+濃度の増加が認められた。
ミツバチTRPチャネルの温度応答性の陽性コントロールとしてショウジョウバエで熱刺激感受性を欠失した変異体の原因遺伝子painlessを強制発現させたHEK296細胞を用いた。Painless遺伝子を導入したHEK293細胞はCa2+イメージング法において熱刺激に対して細胞内Ca2+濃度の大きな増加が観察され,パッチクランプ法でも熱活性化電流が観察された。
野口光一,戴毅(兵庫医科大学医学部)
富永真琴(生理学研究所・岡崎統合バイオサイエンスセンター)
2003年に侵害性冷刺激受容体として遺伝子クローニングされたTRPA1は,その後複数の侵害刺激 (わさび,マスタードオイル,シナモンなど)によって活性化される侵害刺激受容の中心的分子として注目されている。抗TRPA1ポリクローナル抗体を作成 して,Westernblotting法によってTRPA1蛋白質を認識することを確認した。ラット後根神経節をその抗TRPA1抗体を用いて染色し,陽 性細胞が小径の細胞であること,陽性細胞が有髄神経のマーカーであるNF200の抗体で染色されないこと,TRPV1陽性細胞でのTRPA1陽性率が高い こと,炎症に関連するPAR2受容体陽性細胞とも重なりが大きいことを明らかにした。PAR2受容体の特異的刺激剤によってTRPA1活性が増強すること がTRPA1を強制発現させたHEK293細胞,ラット後根神経節細胞でパッチクランプ法を用いた解析によって明らかになった。このTRPA1機能増強に はPIP2量の減少が関与していることが示唆された。
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
関係論文
金田 誠(慶應義塾大学医学部)
霜田 幸雄(東京女子医科大学総合研究所)
鍋倉 淳一(生理学研究所)
コリン作動性アマクリン細胞には複数のClトランスポーター (K-Cl and Na-K-Cl cotransporters) が存在し,その樹状突起上の分布がトランスポーターごとに異なることが網膜神経節細胞の方向選択性の形成に関係しているのではないかとの仮説が提唱されて いる。しかしながらコリン作動性アマクリン細胞に実際どのようなC1トランスポーターが存在し,またその局在がどうなっているのかという点について,形態 学的にまったく明らかにされていなかった。そこで本共同研究ではコリン作動性アマクリン細胞に存在するClトランスポーターを免疫組織化学的手法を用いて 形態学的に同定し,その樹状突起上の分布を明らかにすることを目的として実験を行った。KCC2の分布を共焦点顕微鏡を用いて検討した。
KCC2抗体に対する免疫反応は内顆粒層,内網状層,神経節細胞層で陽性であった。特に内網状層で陽性 反応が最も強く,GFPでラベルされたコリン作動性アマクリン細胞の樹状突起との重なりが観察された。また,内顆粒層と神経節細胞層では細胞体表面で免疫 反応陽性像が観察された。以上の結果から,マウス網膜内網状層ではコリン作動性アマクリン細胞樹状突起上にKCC2が存在する可能性が示唆された。コリン 作動性アマクリン細胞樹状突起が保存されているフラットマウント標本を用いて,共焦点顕微鏡を用いてGFPとKCC2の共存をもとに樹状突起上の分布を検 討することにした。しかしながらフラットマウント標本ではコリン作動性アマクリン細胞樹状突起同士の重なりが激しく,GFP陽性像をもとにした一本の樹状 突起の同定は困難であった。そこでGFP陽性像をもとに同定した単一コリン作動性アマクリン細胞にbiocytinを注入して再染色し,共焦点顕微鏡を用 いてbiocytinとKCC2の免疫反応の重なりを形態学的に同定し,コリン作動性アマクリン細胞樹状突起上のKCC2の分布の観察を予定している。
【追加情報】(調査月2007年8月、記入月2008年6月)
関係論文
竹林浩秀,池中一裕(生理学研究所 分子神経生理研究部門)
冨田江一,平林真澄(生理学研究所 遺伝子改変動物作製室)
胎仔期中枢神経系では,特定の転写因子のセットが領域特異的に発現することにより神経幹細胞に位置情報 を与える。そして,特定の領域より特定の細胞種が産生される。我々が同定したbasic helix-loop-helix型の転写因子Olig2,Olig3の神経発生における機能と,これらの転写因子を発現する細胞の細胞系譜について,詳 細に解析するためにOlig2-CreノックインマウスおよびOlig3-lacZ ノックインマウスの作製を試みた。それぞれの組換えES細胞を8細胞期のICRマウス胚に注入したのち,仮親マウスに移植してキメラマウスを作製した。今 回使用した組換えES細胞からは,比較的低いキメラ率のマウスが生まれた(毛色から推測すると,高いものでも40%程度のES細胞寄与率であった)。これ らのうち一匹のOlig3-lacZキメラマウスから,ES細胞由来のマウスが生まれ,Germ Line Transmissionを確認することができた。
現在,Olig3-lacZヘテロマウス同士の交配により,ノックアウトマウスを作製することを試みている。また,Olig2-Creキメラマウスの交配を継続して行い,Germ Line Transmissionが起こるかどうか経過観察中である。
箕越靖彦,岡本士毅,鈴木敦,志内哲也,李順姫
(生理学研究所生殖・内分泌発達機構研究部門)
冨田江一,平林真澄
(生理学研究所 遺伝子改変動物作製室)
生体のエネルギー代謝を制御するAMPK(AMP -activatedproteinkinase) には,現在複数の関連因子が単離・報告されている。ARK5は,AMPKの触媒体サブユニットファミリーに属する因子であり,現在までに悪性腫瘍での特異 的発現や腫瘍細胞の生存・浸潤・転移活性誘導が報告されている腫瘍悪性化関連因子である。その発現は広く悪性腫瘍に認められるが,脳・骨格筋・心臓等,幾 つかの非腫瘍組織でも認められる。また最近我々は,肥満動物の脂肪組織においてARK5が新規に発現誘導されていることを見いだした。培養細胞を用いた研 究から,骨格筋細胞においてARK5は糖取込みを促進し,脂肪細胞ではインスリン感受性にも関与することを見出した。このようにARK5は,腫瘍悪性化に 加えメタボリック・シンドロームへの関与が考えられる。この可能性をより確かなものにするためには,遺伝子改変動物を使用した研究が非常に有効である。
そこで本研究では,組織特異的プロモーター(骨格 筋:humanskeletalmuscleactin;脂肪細胞:AP2)を用い,マウス骨格筋または脂肪細胞に dominantnegative(DN)-ARK5を発現させ,糖・脂質代謝にどのような影響を及ぼすかを調べることを目的として共同研究を進めてい る。我々は,ARK5の制御領域欠損した触媒体領域のみかつ活性中心となるスレオニン残基のアラニン変換変異体が dominantnegative(DN) として機能することを見いだしているので,これをDN-ARK5として用いた。
ごく最近,行動・代謝分子解析センター,遺伝子改変動物作製室において骨格筋特異的発現DN-ARK5トランスジェニック (Tg) マウス(F0世代)の作成が完了したので,今後Tgマウス・ラインの確立を行った後,インスリン感受性や糖・脂質代謝の変化を解析する予定である。
<<最新の採択表に戻る