細胞器官研究系
概要
細胞器官研究系は生体膜研究部門,機能協関研究部門,神経細胞構築研究部門(客員研究部門)および,細胞生理研究部門(岡崎統合バイオサイエンスセンターとの兼任研究部門)の4部門からなり,分子・細胞レベルから組織・器官レベルへの統合を目指した研究を活発に進めている。特に,チャネル,トランスポーター,レセプター,センサー,酵素などの機能タンパク質と,それらの分子複合体(超分子)の構造と機能及びその動作・制御メカニズムの解明を目指している。また,それらの異常・破綻による病態や細胞死メカニズムの解明に向けて研究を進めている。さらに,神経細胞の大脳皮質構築の基本原理解明に向けた研究を展開している。
各部門においては専門性の高い世界最先端の研究技術(分子細胞生物学,生化学・プロテオミクス,電気生理学,神経解剖学,分子遺伝学)が駆使されている。これら技術を互いに共有し発展させることにより,人体の生命活動の統合的理解を目指す。
本研究部門では膜蛋白質とりわけ脳のシナプス膜に局在する機能蛋白質(神経伝達物質受容体,イオンチャンネル,接着分子など)に焦点をあて研究をおこなっている。シナプス膜蛋白質は単独で機能するのではなく,足場蛋白質,シグナル蛋白質などと複合体(機能ユニット)を形成して,その機能を遂行する。これらの多くのシナプス蛋白質はパルミトイル化脂質修飾を受け,そのシナプス膜における局在が動的に制御されている。私たちは最近発見したパルミトイル化酵素を手がかりとしてシナプス蛋白質の局在,動態制御機構の解明を目指している。一方,独自に開発してきた特異性の高い生化学的技術を駆使して脳組織からシナプス蛋白質複合体(とりわけ疾患候補蛋白質に着目して)を精製,同定し,シナプス伝達効率を制御する機構を統合的に解明することを目指している。
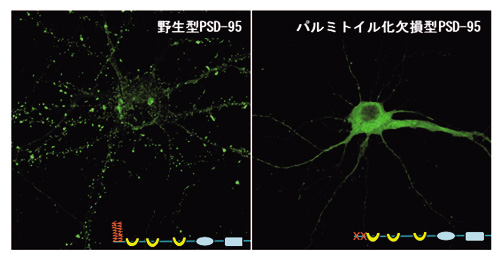 |
図1 パルミトイル化は多くのシナプス蛋白質の局在を制御する
足場蛋白質PSD-95はポストシナプスに濃縮しクラスターを形成するが,3番目と5番目の2つのシステインをセリンに置換(XX)してパルミトイル化修飾を受けないようにしたパルミトイル化欠損型PSD-95は樹状突起,軸索,細胞体全体に無秩序に拡散している。パルミトイル化酵素と脱パルミトイル化酵素のバランスによりPSD-95はダイナミックに局在が変化し,様々な膜蛋白質(例えばAMPA型グルタミン酸受容体)のシナプス局在を制御する。神経活動(外界シグナル)によりパルミトイル化酵素がどのように制御されているかは重要な課題である。
|

|
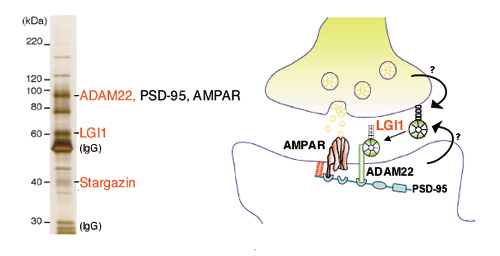 |
図2 てんかん関連蛋白質ネットワーク
代表的なシナプス蛋白質PSD-95を中心とする蛋白質複合体をラット脳から精製し,主要構成蛋白質としてLGI1,ADAM22およびStargazinを同定した(左)。これら3つの蛋白質は遺伝学的にいずれもてんかん発症に関連した蛋白質であった。また,分泌蛋白質LGI1はADAM22と結合することによりAMPA型グルタミン酸受容体の機能を促進した。このように特異性高く蛋白質複合体を精製,同定し,シナプス伝達機構等の様々な生理機能を明らかにしていく。
|
職 員
 |
教 授 深 田 正 紀 FUKATA, Masaki
神戸大学医学部卒,広島大学大学院医学系研究科修了,博士(医学)。日本学術振興会特別研究員(名古屋大学),名古屋大学助手,カリフォルニア大学サンフランシスコ校博士研究員,国立長寿医療センター研究所省令室長を経て平成19年6月から現職。
専攻:神経科学,生化学,細胞生物学。
|
 |
准教授 深 田 優 子 FUKATA, Yuko
神戸大学医学部卒,奈良先端科学技術大学院大学バイオサイエンス研究科修了,博士(バイオサイエンス)。日本学術振興会特別研究員(名古屋大学),カリフォルニア大学サンフランシスコ校博士研究員,国立長寿医療センター研究所特任研究員,生理学研究所専門研究職員,さきがけ研究者を経て平成19年12月から現職。
専攻:神経科学,生化学,細胞生物学。
|
 |
助 教 松 田 尚 人 MATSUDA, Naoto
大阪大学医学部卒,東京大学大学院医学系研究科中退,博士(医学)。東京大学助手,カリフォルニア大学バークレー校博士研究員を経て,平成20年7月1日から現職。
専攻:神経科学。
|
 |
特任助教 岩 永 剛 IWANAGA, Tsuyoshi
秋田大学鉱山学部卒,秋田大学鉱山学研究科修士課程修了,広島大学大学院生物圏科学研究科博士課程修了,博士(学術)。国立循環器病センター研究所派遣研究員,京都大学特任助手,国立長寿医療センター研究所流動研究員を経て平成20年2月から現職。
専攻:分子生物学,生化学。
|
 |
日本学術振興会特別研究員 堤 良 平 TSUTSUMI, Ryouhei
北海道大学理学部卒,同大学院理学研究科修士課程修了,同大学院理学研究科博士課程修了。博士(理学)。国立長寿医療センター・外来研究員を経て平成19年4月から現職。
専攻:細胞生物学,生化学。
|
 |
日本学術振興会特別研究員 則 竹 淳 NORITAKE, Jun
マサチューセッツ大学理学部卒,名古屋大学大学院医学系研究科修士課程修了,同大学院医学系研究科博士課程修了,博士(医学)。日本学術振興会特別研究員(名古屋大学)を経て平成19年4月から現職。
専攻:神経科学,細胞生物学。
|
脳神経系など生体機能のもととなる細胞機能のすべては,細胞膜におけるチャネル(イオンチャネル,水チャネル)やトランスポータ(キャリア,ポンプ),バイオ分子センサーの働きによって担われ,支えられている。私達は容積調節や吸収・分泌機能や環境情報受容,網膜における光受容と視覚情報処理など最も一般的で基本的な細胞活動のメカニズムを,チャネル,トランスポータ,レセプター,センサー,メッセンジャーなどの機能分子の働きとして細胞生理学的に解明し,それらの異常と疾病や細胞死との関係についても明らかにしようとしている。主たる研究課題は次の通りである。
(1)「網膜における視覚情報処理のメカニズム解明」:網膜には,光感受性センサーなど様々な種類のバイオ分子センサーが発現し,初期の視覚の形成を担っている。とくに網膜神経節細胞での視覚情報の統合処理について,網膜組織培養法(図1)を活用したバイオ分子センサーの遺伝子操作および電気生理学的手法を用いて明らかとする。
(2)「細胞容積調節の分子メカニズムとその生理学的役割」:細胞は(異常浸透圧環境下においても)その容積を正常に維持する能力を持ち,このメカニズムには各種チャネルやトランスポータやレセプターの働きが関与している(図2)。これらの容積調節性膜機能分子,特に外向整流性容積感受性クロライドチャネル(VSOR)やそのシグナルの分子同定を行い,その活性メカニズムと生理学的役割を解明する。
(3)「アポトーシス,ネクローシス及び虚血性細胞死の誘導メカニズム」:容積調節能の破綻は持続性の容積変化をもたらして細胞死を誘導する(図3)。多くの細胞のアポトーシス,ネクローシス,更には脳神経細胞や心筋細胞の虚血性細胞死の分子メカニズムを解明する。特に,イオンチャネルの関与とそのメカニズムを明らかにし,「細胞死の生理学」という分野を切り開く。
(4)「バイオ分子センサーチャネルの分子メカニズムの解明」:イオンチャネルはイオン輸送や電気信号発生のみならず,環境因子に対するバイオ分子センサーとしての機能を果たし,他のチャネルやトランスポータ制御にも関与する多機能性蛋白質である。特に,アニオンチャネルやATPチャネルやTRPカチオンチャネルの容積センサー機能,メカノセンサー機能およびストレスセンサー機能の分子メカニズムを解明する。
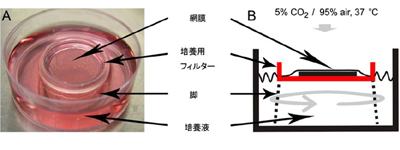 |
| 図1:網膜組織培養系(遺伝子導入)システム |
|
|
|
|
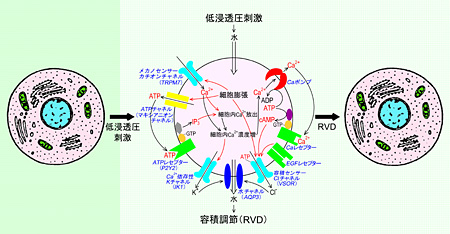 |
| 図2:低浸透圧環境下での細胞容積調節(RVD:調節性容積減少)のメカニズムとVSOR Clチャネルの容積センサー機能 |
|
|
|
|
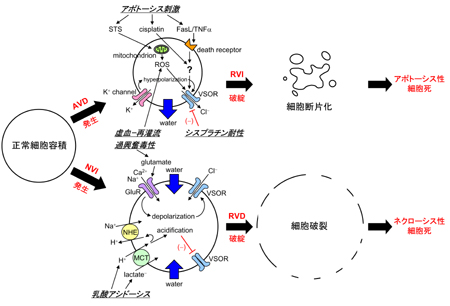 |
| 図3:細胞容積調節破綻とアポトーシス性及びネクローシス性細胞死(RVI:調節性容積増加,AVD:アポトーシス性容積減少,NVI:ネクローシス性容積増加,VSOR:容積感受性Cl-チャネル) |
|
|
|
|
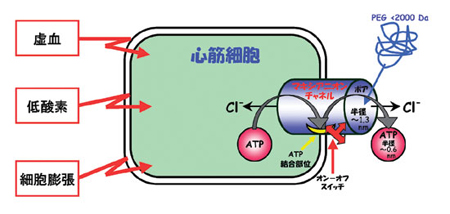 |
| 図4:心筋細胞におけるストレスセンサーATPチャネル |
職 員
 |
所 長 岡 田 泰 伸 OKADA,Yasunobu
京都大学医学部卒,医学博士。京都大学医学部講師を経て平成4年9月から生理研教授。平成16年4月より生理研副所長と併任。平成19年4月より現職。
専攻:分子細胞生理学,細胞死の生理学。
|
 |
准教授 (併任) 小 泉 周 KOIZUMI, Amane
慶應義塾大学医学部卒,医学博士。慶應大学医学部(生理学教室)助手,平成14年米国マサチューセッツ総合病院,Howard Hughes Medical Institute,ハーバード大学医学部研究員を経て平成19年10月から生理研准教授。
専攻:神経生理学,視覚生理学。
|
 |
助 教 久木田 文 夫 KUKITA, Fumio
東京大学理学部物理学科卒,同大学院博士課程修了,理学博士。昭和52年12月から現職。
専攻:神経の生物物理学,神経生理学。
|
 |
助 教 樫 原 康 博 KASHIHARA, Yasuhiro
富山大学文理学部卒,九州大学大学院理学研究科博士課程修了,理学博士。昭和58年7月から現職。
専攻:神経生物学。
|
 |
助 教 毛 利 達 磨 MOHRI, Tatsuma
東京工業大学大学院総合理工学研究科博士課程修了,理学博士。スタンフォード大学ホプキンス海洋研究所,マイアミ大学,カリフォルニア大学デービス校博士後研究員を経て平成8年4月から現職。
専攻:細胞生物学,細胞生理学。
|
 |
特任助教 秋 田 天 平 AKITA, Tenpei
佐賀医科大学医学部卒,名古屋大学大学院医学系研究科博士課程修了,医学博士。日本学術振興会特別研究員,名古屋学芸大学特別研究員を経て,平成20年6月から現職。
専攻:細胞生理学,神経生理学。
|
 |
研究員 浦 本 裕 美 URAMOTO,Hiromi
日本女子大学家政学部卒,総合研究大学院大学生命科学研究科博士課程単位取得退学,理学博士。科学技術振興機構研究員を経て,平成16年4月から現職。
専攻:細胞生理学。
|
神経細胞構築部門のゴールは大脳皮質構築の原理の解明である。一つの研究の焦点として長距離線維連絡の単一軸策の再構築と,その定量的解析を行っている。またこれに関連して,錐体細胞のタイプ分類,シナプスのターゲット特異性と微小回路,そしてこれらの要素がどのように領野特異的な機能構造特性に関連しているかを研究している。我々はこれらの研究のために,分子生物学的テクニック,共焦点および電子顕微鏡,in vitro細胞内電気記録とそれによる細胞染色を含むシステム的神経解剖学的手法を用いている。
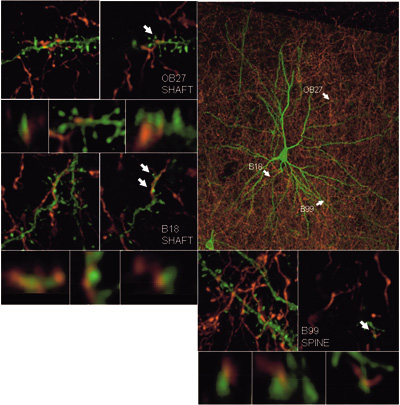 |
サルの皮質連合野に関して,長距離線維連絡の微小回路に関する情報はいまだに極めて少ない。この問題は,現在,BDAを用いたアクソンのラベル(図中赤:streptoavidin Alexa-Fluor 594による)とEGFPによるそのアクソンのターゲットニューロンの可視化(図中緑:Alexa 488 二次抗体による)によって解剖学的にアプローチ可能である。神経細胞によるEGFP発現は,アデノウィルス・ベクターの注入部位のアクソンから取りこまれ逆行性に感染した細胞におこる (Tomioka and Rockland, 2006)。
低倍率の図(右上)は皮質2層のEGFP発現ニューロンを示す。高倍率の図は,低倍率の図の3つの矢印部分の拡大図で,EGFP発現ニューロンの基底樹状突起または尖頭樹状突起の分枝にBDA標識アクソンの接触(シナプス結合が想定される)を示している。高倍率の図は,共焦点顕微鏡図の積み重ね像,1スライス像,3つの接触部位の3次元投影像をそれぞれ示す。
|
職 員
 |
教 授 ROCKLAND, Kathleen ROCKLAND, Kathleen
1979ボストン大学大学院博士課程修了,1983-1991ボストン大学医学部解剖学講座助教授(1983-1987客員として),1991-2000アイオワ大学神経学講座準教授(1991より),教授(1994より),2000-現在 理研・脳科学総合研究センター・チームリーダー,2007-現在,生理研客員教授。
専攻:大脳皮質の神経解剖。
|
分子細胞生物学的,生化学的,発生工学的,電気生理学的手法を用いてTRPチャネルを中心とした温度受容・痛み刺激受容・味覚受容の分子機構の解明,オレキシン神経に焦点をあてた睡眠・覚醒の分子機構の解明を目指して研究を行っている。
- 温度受容の分子機構の解明に関する研究:既知の温度受容体の異所性発現系を用いた解析,変異体等を用いた構造機能解析,感覚神経細胞等を用いた電気生理学的な機能解析,組織での発現解析,遺伝子欠損マウスを用いた行動解析を通して温度受容機構の全容解明を目指している。また,体温近傍の温度でのイオンチャネル活性化の生理学的意義の検討も進めている。さらに,新規温度受容体の探索も進めている。
- 痛み刺激受容の分子機構の解明に関する研究:主に感覚神経細胞,異所性発現系を用いて感覚神経終末における侵害刺激受容の分子機構を明らかにする。この研究には,遺伝子欠損マウスの行動薬理学的解析も行う。
- 体温調節,摂食行動や睡眠覚醒調節などの生体恒常性維持に重要な視床下部神経細胞を中心に解析を行なっている。様々な遺伝子改変動物を作成し,それらを用いてスライスパッチクランプをはじめとする電気生理学的解析や,インビボ細胞外記録,免疫組織化学,睡眠解析などの多岐にわたる手技を組み合わせた解析を行なっている。生命活動の基本を司る神経機構の動作原理を分子レベル,細胞レベル,個体レベルのすべてにおいて明らかにすることを試みている。
|
![[哺乳類の温度感受性TRPチャネル(上)とその性質(下)]](images/12204-01.jpg)
|
[哺乳類の温度感受性TRPチャネル(上)とその性質(下)]
|

|
|
|
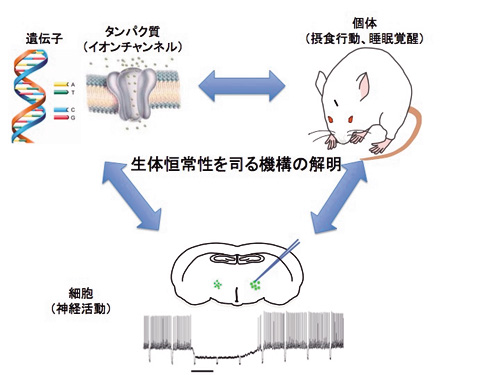
[摂食行動や睡眠覚醒などの調節メカニズムを,分子,細胞,個体レベルのすべてにおいて解明する]
|
職 員
 |
教 授 富 永 真 琴 TOMINAGA, Makoto
愛媛大学医学部卒,京都大学大学院医学研究科博士課程修了,博士(医学)。生理学研究所助手,カリフォルニア大学サンフランシスコ校博士研究員,筑波大学講師,三重大学教授を経て平成16年5月から現職。
専攻:分子細胞生理学。
|
 |
准教授 山 中 章 弘 YAMANAKA, Akihiro
静岡県立大学薬学部卒,筑波大学医学研究科修了,博士(医学)。筑波大学薬理学研究室助手,講師,日本学術振興会海外特別研究員(米国エール大学)を経て平成20年2月から現職。
専攻:薬理学,神経科学。
|
 |
助 教 柴 崎 貢 志 SHIBASAKI, Koji
宇都宮大学農学部卒,九州大学大学院農学研究科修了,総合研究大学院大学生命科学研究科修了,博士(理学),米国ロチェスター大学博士研究員を経て,平成16年9月より現職。
専攻:分子神経生物学。
|
 |
特任助教 曽我部 隆 彰 SOKABE,Takaaki
姫路工業大学(現兵庫県立大学)理学部卒,東京大学大学院医学系研究科博士課程修了,博士(医学)。東京大学学術研究支援員,生理学研究所非常勤研究員,日本学術振興会特別研究員を経て平成20年10月から現職。
専攻:分子細胞生物学。
|
 |
日本学術振興会外国人特別研究員
ボウダカ アッマール BOUDAKA, Ammar
リビア アラファト大学医学部卒,岐阜大学大学院連合獣医学研究科修了,博士(獣医学)。ドイツエルランゲン-ニュルンベルグ大学博士研究員,岡崎統合バイオサイエンスセンター研究員を経て平成20年10月から現職。
専攻:分子細胞生理学。
|
 |
日本学術振興会特別研究員 小 松 朋 子 KOMATSU, Tomoko
金沢大学薬学部卒,金沢大学大学院自然科学研究科修了,総合研究大学院大学生命科学研究科修了,博士(理学)。基礎生物学研究所研究員,岡崎統合バイオサイエンスセンター研究員を経て平成21年4月から現職。
専攻:生化学。
|
 |
研究員 齋 藤 茂 SAITO, Shigeru
弘前大学理学部卒,東京都立大学大学院理学研究科修了,博士(理学)。岩手大学農学部研究員,岩手大学21世紀COEプログラム研究員を経て,平成21年4月から現職。
専攻:分子進化学, 比較ゲノム学。
|
 |
研究員 梅 村 徹 UMEMURA, Toru
名古屋大学理学部卒,名古屋大学大学院理学研究科修了,博士(理学)。名古屋大学研究員,米国ラトガス大学研究員,国立遺伝学研究所研究員をへて,平成20年1月から現職。
専攻:分子生物学。
|
|






















![[哺乳類の温度感受性TRPチャネル(上)とその性質(下)]](images/12204-01.jpg)








