ポストゲノム時代の到来により,脳機能のような複雑な生物反応機構の解明に科学がどこまで迫れるかが問われることになった。よって,外科的手術が容易で,脳地図の解析が進み,かつ心理生理学的解析にも汎用されているマウス・ラットが,今後ますます分子レベルの研究に利用されてくるだろう。遺伝子改変動物作製室では,遺伝子改変動物 (マウス,ラット) の作製技術を提供しつつ,内在性の遺伝子を狙って破壊したノックアウトラット作製技術(マウス以外では作製不可能)の開発,外来遺伝子を導入したトランスジェニックラット作製の効率改善,ならびに作製したノックアウトマウスやトランスジェニックマウス・ラットを利用した大脳皮質第一次視覚野に存在するカラム構造の形成メカニズム・発達メカニズムの解明を目的として,以下の研究を行っている。
(1)精子幹細胞を利用したノックアウトラット作製技術の確立
哺乳類の精巣に存在する精子幹細胞は,個体の遺伝情報を子孫に伝えることができる唯一の幹細胞である。精子幹細胞の分化方向性は決まっているものの,無限に増殖するという点はES細胞と共通している。マウスの培養精子幹細胞(Germline stem cells: GS細胞)は,長期に渡り精子形成能を保持したまま増殖し,精細管内移植すれば正常な子孫作製に寄与しうる精子を形成できると証明されている。また,マウスGS細胞に遺伝子トラップ,ターゲティングの二つの方法で遺伝子導入を行うことにより,ノックアウトマウスが作製できることも報告されている。ラットにおいてGS細胞を樹立し,精細管内移植に適したレシピエント精巣のニッチ環境を調べることを通し,ノックアウトラットの作製方法を確立しようとしている。
(2)トランスジェニックラット作製の効率化
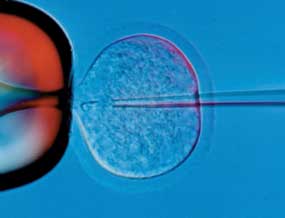
外来DNAを前核期卵子に顕微注入する方法,および精子に外来DNAを付着させて顕微授精する方法のいずれでも,トランスジェニック動物が作出される割合は著しく低い。外来DNAの導入卵子は細胞周期がG1ステージに入るたびに発生遅延・阻害を受けることから,この現象の原因を追究しつつその回避策を模索している。発生阻害を受けずに分娩に至る個体数を増やすことを狙い,結果的に総処理卵子に対するトランスジェニックラットの作製効率を改善しようとしている。
(3)大脳皮質第一次視覚野に存在するカラム構造の形成メカニズム・発達メカニズムの解明
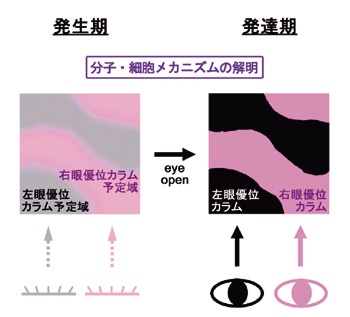
大脳皮質第一次視覚野には,カラム構造をした機能ユニットが多く存在する。中でも,遠近感の知覚に重要と考えられる眼優位カラムは,発生研究および可塑性研究の一番の対象である。この眼優位カラム構造は,出生前後の発生期に大まかに形成され,その後の発達期,外部からの視覚入力によって機能的なカラム構造へと可塑的に構築される。しかしながら,この過程における詳細な分子メカニズム・細胞メカニズムは明らかにされていない。当教室では,発生期から発達期にかけて,このカラム構造に特異的に発現している因子群の単離に成功した。ノックアウトマウスおよびトランスジェニックマウスのシステムを利用して,この因子群の機能解析を行うことで,発生期から発達期における,眼優位カラム形成を司る分子メカニズムを明らかにする。さらに,この因子群のプロモーター下に蛍光タンパクを発現させたトランスジェニックマウスを作製し,発生期から発達期にかけて,この動物の眼優位カラム構築の変遷を追跡することで,眼優位カラム形成の細胞メカニズムを探る。
|