分子生理研究系
概要
分子神経生理研究系は3つの研究部門(神経機能素子研究部門,分子神経生理研究部門,ナノ形態生理研究部門)から成り立っており,生理学研究所「研究の5本の柱」のうち,主に「機能分子の動作・制御機構の解明」を担当している。また,ナノ形態生理研究部門を中心に「四次元脳・生体分子統合イメージング法の開発」にも参加している。
神経機能素子研究部門
イオンチャネル,受容体,G蛋白質等の膜関連蛋白は,神経細胞の興奮性とその調節に重要な役割を果たし,脳機能を支えている。本研究部門では,これらの神経機能素子を対象として,生物物理学的興味から「その精妙な分子機能のメカニズムと動的構造機能連関についての研究」に取り組み,また,神経科学的興味から「各素子の持つ特性の脳神経系における機能的意義を知るための脳スライス・個体レベルでの研究」を目指している。
具体的には,分子生物学的手法により,神経機能素子の遺伝子の単離,変異体の作成,蛍光蛋白やマーカーの付加等を行い,卵母細胞,HEK293細胞等の遺伝子発現系に再構成し,パッチクランプ等の電気生理学的手法,細胞内Ca2+イメージング・全反射照明下でのFRET計測等の光生理学的手法,細胞生物学的手法により,その分子機能を解析している。また,外部研究室との連携により,構造生物学的アプローチ,遺伝子改変マウスの作成も進めている。
研究課題は以下の通りである。
- 内向き整流性K+チャネルの構造機能連関と,異なるサブファミリーに属するサブユニットのヘテロ会合
- 代謝型グルタミン酸受容体の多価陽イオン感知機能の分子基盤と生理的意義,およびマルチパスシグナリングの調節機構
- 膜機能蛋白のサブユニット会合および動的構造変化のFRET法による光生理学的解析
- KCNQ1チャネルとKCNEサブユニットの会合による膜電位センサーの動きの変化,および会合のストイキオメトリーの単一分子蛍光ブリーチ法による解析
- イオンチャネル型ATP受容体P2X2の膜電位依存性ゲートの分子基盤
- 膜電位−細胞長変換素子プレスチンの機能複合体の分子同定と動的構造変化の解析
- マウスTRPA1チャネルのカフェインに対する感受性の質的種間差異の分子基盤
- 小脳プルキンエ細胞のGABAB受容体刺激により活性化するCs+透過型K+チャネルの分子同定
- 代謝型Orphan受容体Prrt3の発現パターンの解析と機能同定
- G蛋白質調節因子RGSの機能解析
- P2X2チャネルおよびプレスチンのレコンビナント蛋白の精製と単一粒子構造解析
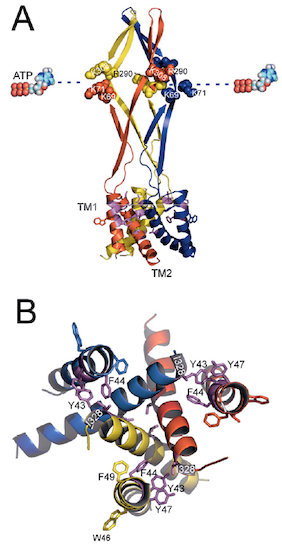
図1 ATP受容体チャネルP2X2の膜電位と [ATP] に依存するゲート機構の構造基盤の同定。変異体解析により同定した重要なアミノ酸残基を,P2X4の結晶構造 (Kawate et al., 2009) に基づいたP2X2のホモロジー構造モデル上にマップした。
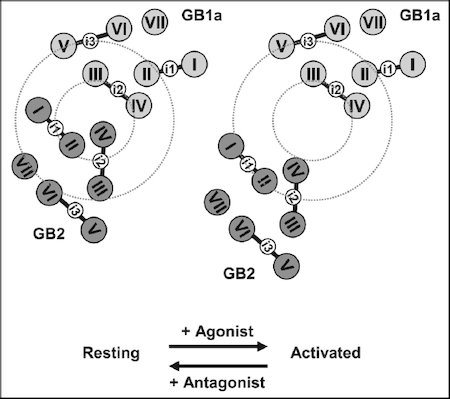
図2 GABAB受容体のリガンド結合に伴うサブユニット配置の変化。
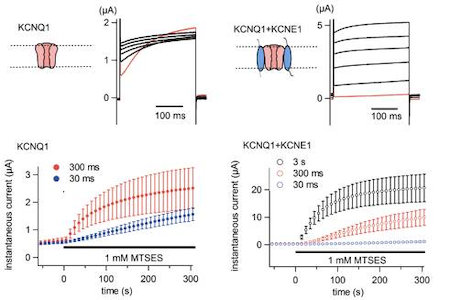
図3 KCNEサブユニット結合によるKCNQ1チャネル電位センサードメインの動きの制御の MTSES accessibility による解析。
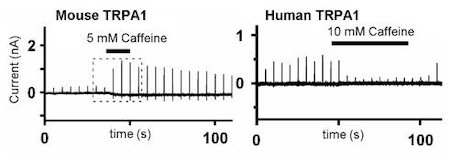
図4 マウスTRPA1チャネルはカフェインにより活性化され,ヒトTRPA1チャネルは抑制される。
職 員
東京大学医学部卒,同医学系研究科博士課程修了,医学博士。カリフォルニア大学サンフランシスコ校・ポスドク,東京都神経科学総合研究所・副参事研究員,東京医科歯科大学医学部・教授を経て,平成15年12月から現職。
専攻:分子生理学,神経生物学。
東京大学薬学部卒,同大学院修了,薬学博士。順天堂大学助手,米国コロンビア大学博士研究員,CREST研究員を経て,平成16年6月から現職。
専攻:薬理学,生理学。
東京大学教養学部卒,同大学院修了,博士(学術)。井上フェロー,生理学研究所非常勤研究員を経て,平成17年4月から現職。
専攻:分子生理学,生物物理学。
Hacettepe 大学医学部卒,同修士課程修了,総研大博士後期課程修了,博士(理学)。平成21年10月から現職。
専攻:分子生理学,生物物理学。
分子神経生理研究部門
(1)神経系の発生過程において,神経系を構成する多くの細胞は共通の前駆細胞である神経上皮細胞から発生・分化してくる。分子神経生理部門では,神経上皮細胞からどのようにして種々の細胞種への分化決定がなされるのか分子・細胞生物学的に研究している。その中でも,グリア細胞の系譜については,未だ不明の点が多く,遺伝子改変マウスの作製,免疫組織学的手法やin situ hybridization法並びにレトロウイルスによる細胞系譜解析を駆使して解析を進めている。また,再生医療を目指して神経幹細胞移植により脱髄マウスを治療することを試みている。
(2)神経上皮層で増殖し分化の方向の決まった細胞は,機能する部位に向かって移動することが知られている。神経系で見られる細胞移動は,大脳や小脳の皮質形成過程でみられるニューロンの放射状移動については詳細に調べられているが,比較的長距離を移動する正接方向への移動やグリア前駆細胞の移動に関しては,不明な点が多い。このような細胞の移動様式や制御機構を明らかにするために,発達途上の脳内に様々な遺伝子を導入して,形態学的に解析している。
(3)神経幹細胞は,脳を構成する全ての神経細胞・アストロサイト・オリゴデンドロサイトの前駆細胞である。発達期の胎仔脳のみならず成体脳にも存在し,成体脳の特定の部位における神経細胞の新生に関与している。神経幹細胞の発生から,増殖・維持・分化さらに老化に至るまでを制御している分子機構を解明し,神経幹細胞の生体内での挙動を明らかにすることを目指している。
(4)脳の発達段階における糖蛋白質糖鎖構造を独自に開発した方法を用いて解析したところ,個人間で極めてよく保存されていることが明らかとなった。現在,脳の領域化や癌の発生・転移におけるN-結合型糖鎖の重要性について研究している。
(5)以上の研究において開発した神経系における遺伝子導入技術を利用して遺伝子治療の基礎的研究を行っている。
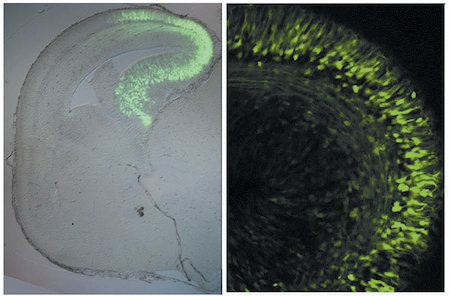
A)エレクトロポレーション法によるマウス胎児脳への遺伝子導入
マウス脳室内に緑色蛍光遺伝子(GFP)発現ベクターを注入した後,エレクトロポレーションを行った胎児脳の限局した領域に効率よく遺伝子導入できることが分かった。
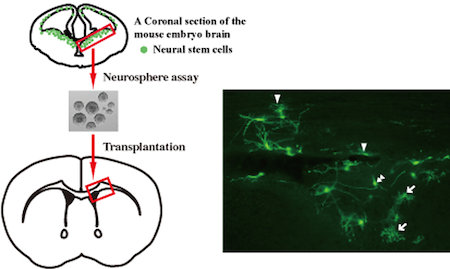
B)神経幹細胞の成体脳への移植
全身でGFPを発現するマウス胎仔脳より神経幹細胞を培養・単離し,成体脳へ移植した。移植から4週間後の脳においてGFP陽性細胞が観察され,形態からアストロサイト(矢印)・オリゴデンドロサイト(矢頭)・神経細胞(2重矢頭)へ分化したことがわかる。

C)ATPとグルタミン酸放出の可視化
I) 培養アストロサイト低浸透圧ストレス負荷時に観察されるATPの放出。ルシフェリン−ルシフェラーゼ反応による発光を利用してATPの局在が可視化できる。
II)同じく低浸透圧ストレス負荷時に観察されるグルタミン酸の放出。Glutamate optic sensorを細胞膜上に固定し(a),グルタミン酸濃度変化に依存した蛍光強度の変化を求めた。正常状態(b)ではグルタミン酸放出は観察されないが,低浸透圧下(c)ではグルタミン酸放出が一つ一つの白い固まりとして可視化出来る。
職 員
大阪大学理学部卒,同大学院理学研究科修了,理学博士。大阪大学蛋白質研究所助手,助教授を経て,平成4年11月から現職。
専攻:分子神経生物学。
東京大学医学部卒,臨床研修および神経内科トレーニングの後,同大学院医学系研究科博士課程修了,医学博士。理化学研究所基礎科学特別研究員,カナダ・トロント大学ポスドク,東京大学医学部助手を経て,平成15年9月から現職。
専攻:神経発生学,臨床神経学。
慶応義塾大学医学部卒,同大学病院精神神経科研修医修了,同大学院医学研究科博士課程修了。医学博士。生理学研究所リサーチ・アソシエイトを経て,平成16年6月から現職。
専攻:神経生化学,精神神経生物学。
九州大学農学部卒,奈良先端科学技術大学院大学を経て,名古屋大学大学院医学系研究科博士課程修了,医学博士。日本学術振興会特別研究員を経て,平成20年11月から現職。
専攻:分子生物学,神経科学。
京都工芸繊維大学繊維学部卒,神戸大学自然科学研究科修士課程を経て,大阪大学理学研究科博士課程にて学位取得(理学)。平成19年10月より現職。
ナノ形態生理研究部門
岡崎統合バイオサイエンスセンター
戦略的方法論研究領域
兼務
新しい学問領域は,新しい方法論の発見・発明によりスタートすることが多い。例えば,現在医学の診断に幅広く使われている磁気共鳴イメージングは,もともと分光装置として誕生した磁気共鳴 (NMR) から生まれ,近年は機能イメージングとして脳研究にまで利用されている。
このように,各学問分野の急速な発展の裏には新しい方法論の発見がある。その方法論が,新しい分野を生み出すきっかけを与え,それがまた新しい方法論を次々に生む。こうした革新的方法論を戦略的方法論と呼ぶ。
統合バイオサイエンスという新しい学際領域は,領域間の単なる和では確立し得ない困難さを持っている。そこで,領域全体を引っ張る新しい方法論のブレークスルーが必要となる。すなわち,従来の方法では見えなかった1分子レベルの3次元構造解析,分子レベルの機能の入出力解析,細胞系のその場の機能観測などを可能にする戦略的方法論が期待されている。
具体的には,以下の研究を行っている。
- 位相差電子顕微鏡の開発と応用−位相観測を可能とする位相差電子顕微鏡(位相差法,微分干渉法,複素観測法)を応用し,蛋白質,ウィルス,オルガネラなどのin vitro 立体構造解析と細胞組織のin vivo 構造生物学を行う。特に“生”状態の神経細胞系の高分解能観察を行うため光顕と電顕の有機的統合手法,光顕−電顕相関法を開発している。
- 物質輸送研究I−水,イオン,基質の経細胞及び傍細胞輸送機構,開口分泌の分子機構とエネルギー供給の分子機構の研究を行う。
- 物質輸送研究II−エンドサイトーシスはゴルジ体への外向き輸送とリソソームへの内向き輸送間の選別装置として働き,細胞内膜系の分子の運命を決定する。このエンドサイトーシス経路をめぐる細胞内膜系の選別輸送の分子機構および細胞のシグナル伝達,極性形成などにおける役割を研究する。
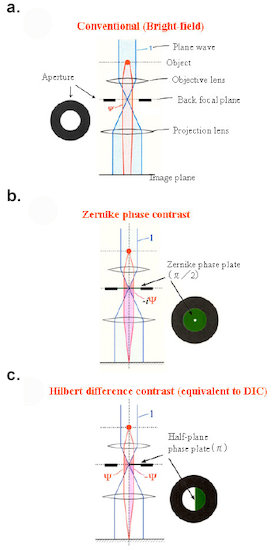
図1.電子位相顕微鏡法の3種
a.焦点はずし(デフォーカス)を導入し,分解能を犠牲にしてコントラストを向上する通常法(明視野法)。
b.ゼルニケ(Zernike)位相版(π/2シフト)を対物レンズ後焦点面に挿入し,正焦点で高コントラストを回復するZernike位相差法。
c.半円位相版(πシフト)を後焦点面に挿入し,微分干渉光学顕微鏡と同じような地形図的位相像を得るヒルベルト(Hilbert)微分法。

図2.2つの電子位相顕微鏡装置
a.300kV分析型極低温電子顕微鏡(FEG,He-ステージおよびエネルギーフィルター搭載)に薄膜位相板を挿入。
b.200kV低温トモグラフィー用電子顕微鏡(FEG, N2- 傾斜ステージ,エネルギーフィルター搭載)に薄膜位相板を挿入。
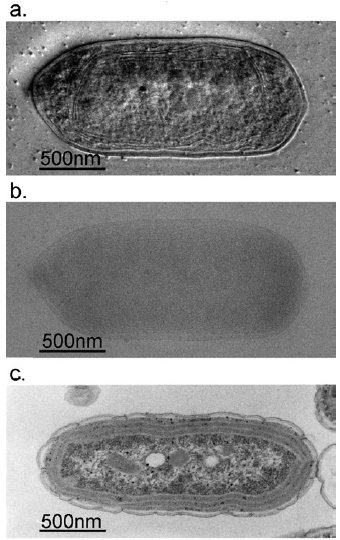
図3.シアノバクテリアの300kV全細胞氷包埋像と100kVプラスチック包埋切片像 (Kaneko et al., J.Electro. Microsc. 54(2005)79)
a.Hilbert微分法で観察したシアノバクテリア300kV氷包埋像。無染色にもかかわらず細胞内構造が2nmの分解能で見える。
b.通常法で同一サンプルを観察したときのシアノバクテリア300kV氷包埋像。コントラストが低いため内部構造を特定できない。
c.固定,脱水,プラスチック包埋,電子染色して得たシアノバクテリアの100kV切片像。化学的処理は時間がかかり(~数日),かつ細胞内構造を破壊する。従って切片像では10nm以下の微細構造を議論するのが困難であった。

図4.インフルエンザAウィルスの2次元および3次元位相差電子顕微鏡像
a.通常2次元像 (300kV)。
b.ゼルニケ位相差2次元像 (300kV)
c.ゼルニケ位相差トモグラム(3次元像)の1断面図 (200kV)
d.ゼルニケ位相差トモグラムより再構成したインフルエンザゲノムの3次元像 (200kV)
(d.の3次元グラフィックスは自然科学研究機構イメージングサイエンス研究分野武田隆顕氏製作)
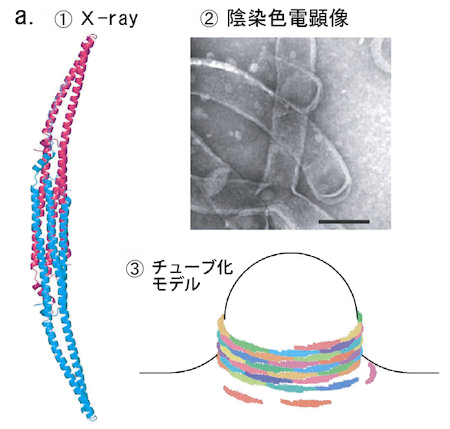
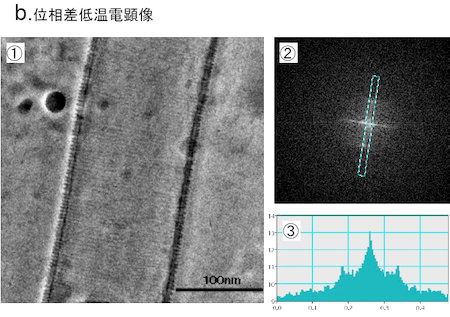
図5.X線結晶解析と通常電顕観察のギャップを埋める位相差低温電顕法
a.脂質相互作用蛋白質PCHのEFCドメイン2量体のX線結晶解析から紐状構造が決定(①)。PCHが脂質のチューブ化にかかわっていることが,陰染色の電顕観察から判明(②)。この2つの知見をもとにチューブ化機構として③のようなモデルが提出された。
b.このモデルを証明する観察が位相差法の適用で明らかになった(①)。フーリエ変換の解析結果(②, ③)から脂質に隙間なく巻きついた蛋白質の間隔は,4nmで,これはX線構造からの推定値と符合した (Shimada et al., Cell , 129(2007)176)。
職 員
東京大学理学部卒,同大学院修了,理学博士。日本電子(株)生体計測学研究室長,科学技術振興事業団プロジェクト総括責任者,東京大学教養学部教授,生理学研究所教授を経て平成13年2月から現職。
専攻:生物物理学,電子線構造生物学,生理現象の熱統計力学。
京都府立医科大学卒,医学博士。大阪医科大学助手,生理学研究所助教授を経て平成15年4月から現職。
専攻:分子生理学,外分泌腺分泌機構とエネルギー供給,傍細胞輸送。
京都大学理学部卒,同大学院修了,理学博士。ドイツ,ハイデルベルク大学研究員,生理学研究所助手を経て平成15年7月から現職。
専攻:細胞生物学。
ソフィア大学(ブルガリア)物理学部卒,同大学修士課程修了,総合研究大学院大学生命科学研究科修了,理学博士。生理学研究所非常勤研究員,日本学術振興会特任助教を経て平成20年4月より現職。
専攻:電子線構造生物学。
神戸大学農学部卒,同大学院自然科学研究科修了,博士(学術)。平成20年4月より現職。
専攻:植物病理学,植物細胞生物学。
信州大学工学部卒,名城大学院理工学研究科修了,博士(工学)。平成20年7月より現職。
専攻:材料工学。
神奈川大学理学部卒,総合研究大学院大学生命科学研究科修了,博士(理学)。平成21年4月より現職。
専攻:神経解剖学。















