発達生理学研究系
概要
発達生理学研究系は,平成15年度より「心と身体の発達における生理学的機構をあきらかにすること」を目的として,専任3部門,客員1部門の研究系として発足した。専任1部門はそれまで統合生理研究施設高次脳機能研究プロジェクト(伊佐正教授)が配置換えで認知行動発達機構研究部門として発足し,眼球や手の運動を制御する神経回路の発達と損傷後の機能代償機構について研究を展開している。また生体恒常機能発達機構研究部門の教授には鍋倉淳一教授が選出され,平成15年より中枢神経系のシナプスの発達および脳損傷後の神経回路のリモデリングのメカニズムを電気生理学的研究手法や多光子顕微鏡などを用いて解析している。また生殖内分泌機能発達研究部門には箕越靖彦教授が選出され,平成15年に着任し,肥満の原因となる視床下部の代謝中枢に関する研究を行っている。また客員研究部門については,平成21年11月1日から矢田俊彦教授(自治医科大学医学部)が環境適応機能発達研究部門の客員教授として着任された。
認知行動発達機構研究部門
認知行動発達機構研究部門では脳による運動制御,特に眼球のサッケード運動系及び手指の物体把持(grasping)運動について大規模及び局所神経回路の構造と機能の解析,さらには損傷時の機能代償機構を研究している。
1.特に眼球のサッケード運動系については
(1)サッケードの制御にとって重要な中枢である中脳上丘の局所神経回路の構造と機能をマウスの脳スライス標本においてパッチクランプ法などを用いて解析する。
(2)麻酔下動物(ラット,サル)における上丘,大脳皮質をめぐる大規模神経回路及び上丘局所神経回路のシナプス機構を解析する。
(3)遺伝子改変マウスにおいてサッケード運動を解析する事を通じてサッケード制御回路の分子機構の明らかにする。
(4)覚醒サルにおける電気生理学,薬物微量注入法を用いてサッケード制御系の動的特性を解析する。
(5)大脳皮質一次視覚野(V1)を損傷したサルを,いわゆる「盲視」の動物モデルとして用い,V1損傷後も障害視野へのサッケード運動を可能とする神経機構の解析,および盲視における「見え(視覚的意識)」とその神経機構を明らかにする。
2.手指の運動については,
我々は霊長類において大脳皮質一次運動野から手指筋運動ニューロンに至る経路には直接結合のほかに頚髄の介在ニューロンを介する間接的な経路も存在することを明らかにした。そして中部頚髄レベルで直接結合を遮断し,間接経路のみを残したサルにおいても1‐3ヶ月の回復期を経て手指の精密把持運動が回復になることを見出した。このモデルを用いて,機能代償の神経機構をPETによる脳活動イメージング,電気生理学,神経解剖学,遺伝子発現解析など様々な手法を解析している。また手や指の運動の正確な制御を可能にする脊髄神経機構を明らかにするため,覚醒行動中のサルの脊髄からの神経活動記録などを行って解析している。
また,最近新たに,運動の制御機構を,「機能を操作」することによって解明することに取り組み始めた。ひとつは,ブレインマシンインタフェース(BMI)によるニューロン活動からの信号の抽出である。もう一つは,ウイルスベクターを用いた遺伝子導入による機能操作であり,例えば,optogeneticsは特定の機能やネットワークを持つニューロンの識別のための強力なツールとなる。
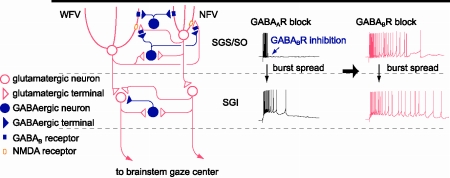
図1 上丘でのGABAB受容体を介したバースト発火の制御機構の模式図。GABAB受容体は上丘浅層のnarrow field vertical cell (NFV)とwide field vertical cell (WFV) のシナプス後膜およびグルタミン酸作動性神経終末に発現している。浅層のGABA作動性ニューロンのバースト発火によって遊離されたGABAが,これらの受容体に作用するとNFVでは過分極が,WFVではシャンティング抑制が誘発され,また,シナプス終末からのグルタミン酸遊離が抑制される。
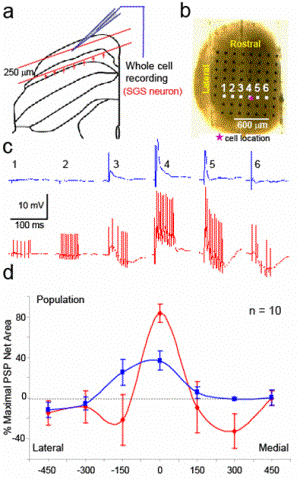
図2 (a) 上丘のtopographic mapに沿って記録および刺激を行うため,上丘浅層の水平断面のスライスを作成する。(b) ピンクの印の位置のニューロンから記録し,白い四角印の部位に刺激を与える。各刺激に対する応答を(c)に示した(上:単一刺激,下:11 パルス/200Hz刺激)。各応答のEPSPおよびIPSPの積分を記録位置から刺激電極までの距離にプロットしている。特に連発刺激に対しては,刺激部位付近ではEPSPが観察され,150-300μm付近ではIPSPが優勢になる,メキシカンハット状の分布応答を示す。
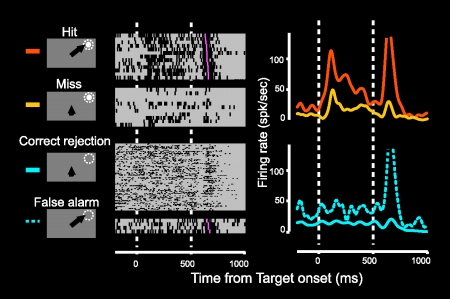
図3 片側一次視覚野除去後のサルから計測された,視覚刺激検出課題遂行中の損傷側上丘の神経活動。損傷側上丘・中間層の神経細胞ではサルの行動と相関した視覚応答の変化が見られる。ターゲットの検出・サッケードによる定位に成功した試行(Hit trial)では明確な視覚応答が観察されるのに対し,サルがターゲットを検出できなかった試行(Miss trial)では,視覚刺激はまったく同じであるにもかかわらず視覚応答は減衰している。
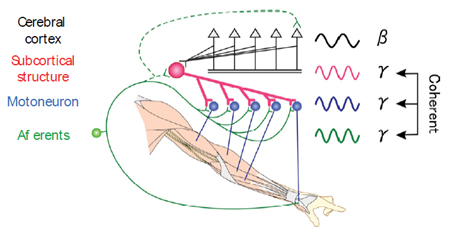
図4 脊髄損傷後の手の器用さの機能回復には,損傷されずに残った皮質下の神経回路内の共通した振動活動が貢献する。
職 員
東京大学医学部卒,同医学系研究科修了,医学博士。スウエーデン王国イェテボリ大学客員研究員,東京大学医学部助手,群馬大学医学部助教授を経て平成8年1月から現職。
専攻:神経生理学。
東京大学薬学部卒,東京大学大学院薬学系専攻博士課程中退,医学博士。科学技術振興事業団心表象プロジェクト研究員,科学研究費(特別推進)研究支援員を経て平成15年6月から現職。
専攻:認知神経科学,神経生理学。
京都大学薬学部卒,同薬学研究科博士課程修了,薬学博士。東京都神経科学総合研究所客員研究員,テネシー大学ポスドクを経て平成17年9月から現職。
専攻:神経生理学,神経薬理学。
東京大学理学部卒,東京大学大学院理学系研究科修士課程修了,東京大学大学院医学系研究科博士課程修了,医学博士。科学技術振興機構研究員を経て平成22年1月から現職。
専攻:神経生理学,認知神経科学。
筑波大学生物学類卒,筑波大学大学院医科学研究科修士課程修了,同医学研究科博士課程修了,医学博士。生理学研究所リサーチアソシエイト,ロックフェラー大リサーチアソシエイト,生理学研究所研究員を経て平成22年2月から現職。
専攻:神経生理学。
大阪大学医学部卒,大阪大学大学院医学研究科修士課程修了,同博士課程中退,博士(医学)。島根大学医学部助手,基礎生物学研究所研究員を経て平成22年4月から現職。
専攻:神経生理学,環境生理学。
日本大学文理学部卒,横浜国立大学大学院教育学研究科修了,千葉大学大学院医学研究科修了,医学博士。生理研研究員を経て,平成19年7月からワシントン大学客員研究員。平成22年10月からさきがけ研究員(JST)。
専攻:神経生理学。
東京理科大学理学部第二物理学科卒,東京大学工学系研究科修士課程,同大学院博士課程修了,工学博士。玉川大学学術研究所研究員,日本学術振興会特別研究員,玉川大学学術研究所OCE助手,同大学脳科学研究所特別研究員を経て平成20年から現職。
専攻:神経科学,生体情報システム工学。
東京大学理学部卒,同大学院修士課程修了,総合研究大学院大学博士課程修了,博士(理学)。生理学研究所研究員,オックスフォード大学客員研究員を経て平成18年8月から現職。
専攻:神経科学。
茨城大学理学部卒,筑波大学医学系研究科修了,医学博士。生理学研究所 非常勤研究員,フランス College de France研究員,科学技術振興機構研究員を経て,平成22年4月より現職。
専攻:神経生理学。
東京大学理学部卒,東京大学大学院理学系研究科修士課程修了,東京医科歯科大学大学院医歯学総合研究科修了,医学博士。COE拠点形成特別研究員を経て平成19年4月から現職。
専攻:神経生理学。
国際基督教大学教養学部卒,京都大学大学院情報学研究科博士課程中退(情報学修士)。(株)クバプロ,日本科学未来館を経て,平成21年1月から現職。
専攻:知能情報学。
チュラロンコン大学(タイ)薬学部卒,総合研究大学院大学博士課程修了,博士(理学)。 平成21年4月から現職。
専攻:神経生理学。
生体恒常機能発達機構研究部門
発達後期には神経回路機能の再編成がおこる。これは既に機能している神経回路における現象であるため,しばしば行動,感覚やリズムなど個体の脳機能の大きな変化として表現される。
この発達期における神経回路機能の再編成のメカニズムを回路およびシナプスレベルで解明する。さらに,この変化に対する個体内外環境による制御機構および関連分子について解明する。また,外傷や虚血などの障害後には未熟期の回路の特徴が再現し,その後の回復期には発達と同じような過程が再現される。
これらの発達期および障害回復期における神経回路の機能と神経回路およびシナプス動態の長期変化について,多光子励起顕微鏡による生体内イメージング法,電気生理学的手法および分子生物学的手法を用い解析を行なっている。また,発達期および障害後のGABA作動性回路の興奮性—抑制性スイッチ変化を引き起こす細胞内クロールイオン濃度調節分子の機能発現機構について検証する。未熟期および障害後にGABAが興奮性である生理的な意義について,細胞内クロールイオン調節分子の生体内調節が可能な遺伝子改変マウスを作製し,検討を加えている。
2光子励起顕微鏡を用いたイメージング技術の高度化のため,レーザー光路系,生体装着アダプター,および蛍光タンパク発現操作技術の改良を行い,大脳皮質の錐体神経細胞,各種グリアおよび血管・血流イメージングの高度化,同一微細構造の数カ月にわたる長期繰り返し観察技術の確立を行った。脳などの生体組織表面から約1mmの世界最深部におけるシナプスなどの微細構造の可視化に成功した。
以下に具体的な研究課題を示す。
(1)2光子励起法による生体イメージング技術により発達および障害後の神経細胞樹状突起やスパインの変化,およびミクログリアによるシナプス監視機構と障害シナプスのリモデリングへの関与について研究を行っている。また,大脳皮質感覚野の梗塞後には対側大脳皮質半球の相同領域(感覚野)において,障害後2週目の限られた期間にシナプスの再編が更新し,障害皮質の機能を代償する回路が作られることを明らかにした。また,慢性疼痛時における大脳皮質感覚野の機能回路のリモデリングについてカルシウムイメージングによる細胞活動やスパインのターンオーバーを指標として検討している。
(2)成熟における代表的抑制性伝達物質であるGABA/グリシンは,未熟期および障害後には脱分極を引き起こす。この機能スイッチに関して,細胞内クロールイオンくみ出し分子であるカリウム−クロール共役分子(KCC2)について,チロシンリン酸化による細胞膜発現パターンおよび内在について,分子生物学,電気生理学およびイメージング技術を用いて検討を進めている。また,成熟期においても視床下部GnRh神経細胞にはKCC2の発現がなく,GABAは脱分極をしめす。細胞および時期特異的なKCC2発現のコントロールが可能な遺伝子改変マウスを作製し,これらGABAの脱分極(興奮性)の生理学的意義を,イメージング,分子生物学および電気生理学的手法を用いて検討している。
(3)我々が報告した新しいカテゴリーの神経回路の発達再編である単一神経終末内での伝達物質自体のスイッチングのメカニズムについて,多角的に解析している。
(4)中枢神経細胞の急性単離法を用いて,TRHなどの各種活性物質の神経伝達および神経細胞の興奮性制御,およびそのメカニズムについて電気生理学的検討を加えている。
職 員
九州大学医学部卒,医学博士,東北大学医学部助手,秋田大学医学部助教授,九州大学医学研究院助教授を経て,平成15年11月から現職。
専攻:神経生理学,発達生理学。
九州大学薬学部卒,同大学院修士課程修了,九州大学大学院医学系研究科博士課程修了,医学博士,熊本大学薬学部講師,九州大学医学系研究科講師を経て,平成19年1月より現職。
専攻:神経生理学。
九州大学医学部卒,医学博士,九州大学医学部(整形外科)助教を経て,平成22年4月から現職。
専攻:神経生理学。
早稲田大学人間科学部卒,同大学院修士課程修了。日本医科大学大学院医学研究科修了。博士(医学)。生理学研究所非常勤研究員を経て,平成18年4月から現職。
専攻:神経科学。
静岡県立大学薬学部卒,九州大学大学院薬学府修士課程修了,同大学院博士課程修了,薬学博士。平成21年4月より現職。
専攻:神経生理学。
慶熙大學韓醫學科卒,同大學院博士課程修了,韓醫學博士。現同大學鍼灸經絡科學硏究所硏究員。現JSPS外國人特別硏究員。
專攻:神經科學。
生殖・内分泌系発達機構研究部門
ヒトをはじめとする動物生体は,内的ならびに外的環境の変化に即応しながらも体内の内部環境をできるだけ一定に保とうとする機構を備えており,広くホメオスタシス(恒常性維持機構)として知られている。とりわけ視床下部は,ホメオスタシスの調節系である自律神経系,内分泌系,免疫系をとりまとめる高位中枢として,個体の生命保持ならびに系統維持のための基本的な諸活動を調整する働きを営んでいる。本研究部門では,ホメオスタシスの中でも,特に,摂食行動とエネルギー消費機構からなる生体のエネルギーバランスに注目し,視床下部が生体のエネルギーバランスに対してどのような調節作用を営んでいるかを明らかにすると共に,その破綻が肥満や糖尿病の発症とどう関わるかを解明することを目指している。主たる研究課題は以下の通りである。
(1)視床下部における摂食行動の調節機構。
(2)糖・脂質代謝に及ぼす視床下部−交感神経系の調節機構。
(3)レプチンなどアディポカインの細胞内シグナル伝達機構。
(4)AMPKとAMPKファミリーの代謝調節作用と病態との関連
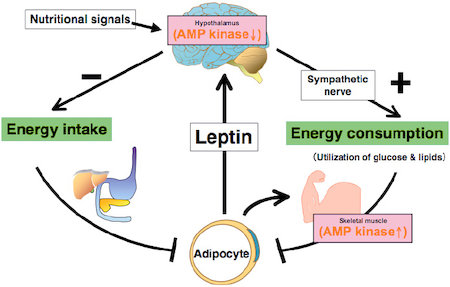
図1:レプチンは視床下部と骨格筋のAMPキナーゼ(AMPK)を相反的に調節することによって生体エネルギー代謝を調節する。
レプチンは,骨格筋のレプチン受容体Ob-Rbを介して直接的に,並びに視床下部—交感神経系を介して間接的に骨格筋のAMPKを活性化し,脂肪酸酸化を促進する。またレプチンは,視床下部AMPK活性を逆に抑制することによって摂食抑制作用を引き起こす。AMPK活性に対するこのような相反的な調節作用は,レプチンによるエネルギー代謝調節作用に必須である。レプチンが視床下部と骨格筋においてどのようにAMPK活性を相反的に調節するかは,重要な研究課題の一つである。
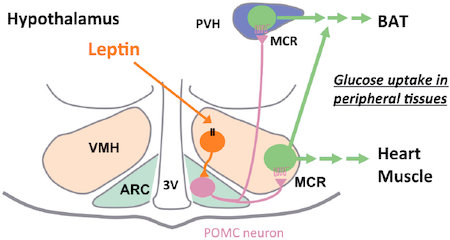
図2:レプチンによる視床下部を介したグルコース代謝調節作用
レプチンは,視床下部腹内側核(VMH)ニューロンを介して弓状核(ARC)POMCニューロンを活性化する。その結果,VMH及び室傍核(PVH)ニューロンに発現するメラノコルチン受容体(MCR)の活性を高める。VMHのMCRは褐色脂肪組織(BAT),心臓,骨格筋のグルコース取り込みを促進する。これに対して,PVHのMCRはBATのグルコース取り込みを選択的に促進する。
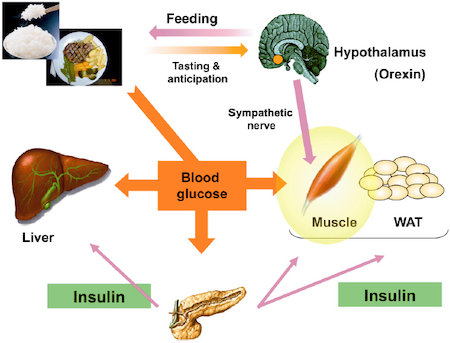
図3:オレキシンによる骨格筋でのグルコース代謝促進作用
オレキシンは,睡眠・覚醒,摂食,動機付け行動を調節する視床下部神経ペプチドである。オレキシンは,摂食時に味覚刺激や食事に対する期待感によって活性化し,VMHニューロンを介して骨格筋でのグルコースの利用を選択的に促進する。骨格筋でのグルコース利用が高まることによって血糖の過度な上昇が抑制される
職 員
愛媛大学医学部卒,愛媛大学大学院医学研究科博士過程終了,医学博士。同大学医学部助手,講師,助教授,ハーバード大学医学部Lecturerを経て平成15年11月から現職。
専攻:代謝・内分泌学。
徳島大学総合科学部卒,同大学院人間自然環境研究科修士課程修了,愛媛大学大学院医学系研究科博士課程修了,医学博士。愛媛大学医学部助手,平成16年3月より現職。
専攻:代謝・内分泌学,運動生理生化学。
北海道大学獣医学部卒,同大学院獣医学研究科博士課程修了,獣医学博士。日本学術振興会特別研究員,東京都臨床医学総合研究所常勤流動研究員を経て平成16年4月から現職。
専攻:神経免疫学,幹細胞生物学。
広島大学生物生産学部卒,名古屋大学医学研究科博士課程修了,医学博士。ノースウエスタン大学,九州大学リサーチアソシエイト,宮崎大学,琉球大学を経て平成22年2月より現職。
専攻:粘膜免疫学。
北海道大学獣医学部卒,総合研究大学院大学生命科学研究科博士課程修了,学術博士。平成21年10月より現職。
専攻:代謝・内分泌学。
環境適応機能発達研究部門(客員研究部門)
インスリン分泌調節:1)グレリンによるインスリン分泌抑制のメカニズム解明と,内因性グレリン阻害によるインスリン分泌促進による2型糖尿病治療の基盤構築。2)β細胞電位依存性Kチャネル(Kv)によるインスリン分泌調節における役割の解明。
摂食調節:1)視床下部,特に一次中枢弓状核から統合中枢室傍核への,摂食調節神経回路の解明。2)新規満腹ペプチドNesfatin-1とオキシトシンによる摂食抑制機構と生理的・病態的・治療的意義の探索。3)脳‐臓器連関による摂食と生体恒常性制御。
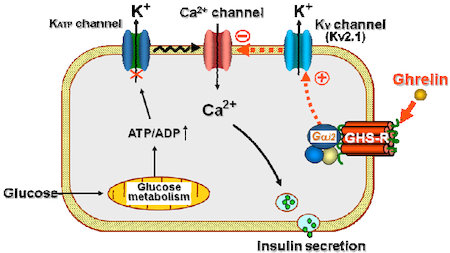
図1 Ghrelinによるインスリン分泌抑制のメカニズム
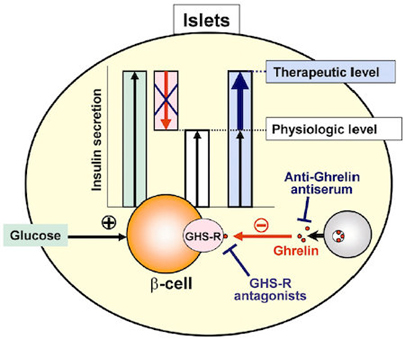
図2 膵島の内因性ghrelinはインスリン分泌を抑制し,その阻害でインスリン分泌が促進される。
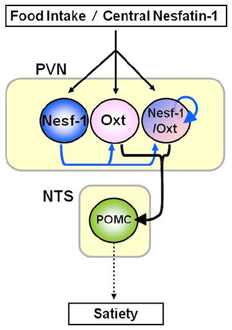
図3 Nesfatin-1作動性PVNオキシトシン神経性シグナルは,NTS POMC神経に働き,メラノコルチン依存性満腹感を引き起こす。
中枢性のNesf-1または食事摂取によってPVNのNesf-1およびOxt神経が活性化される。PVNでは,内因性Nesf-1がOxt神経に対する自己分泌性または局所神経活性物質として作用する。PVNのNTSに対するオキシトシン神経性シグナルはPOMC神経を活性化し,メラノコルチン依存性の満腹感を誘発する。
職 員
1975北海道大学工学部卒業。1983京都大学大学院医学研究科博士課程修了。1983-1987東京医科歯科大学医学部生理学第二講座助手。1986-1987コーネル大学獣医学部薬理学Postdoc. 1987-2000鹿児島大学生理学第一講座助教授。1996-2000岡崎国立共同研究機構生理学研究所細胞内代謝研究部門客員助教授。2000-Professor,自治医科大学生理学講座統合生理学部門教授。2009-自然科学研究機構生理学研究所発達生理学研究系客員教授。
専攻:生活習慣病(糖尿病,肥満,など)の成因解明。
























