TRPM2�`���l�������ߐ��זE�e�ϑ���@�\��S�����Z����
�������z�C�I���`���l��HICC�̕��q���̂ł���Ɠ���
�זE�튯�����n�@�@�\����������
�������̑̂��\������זE�́A��Ɉ��̑傫����ۂ��Ă��܂��B���Ƃ��A�������^���ɂ��E���A�ߏ�ȉ������ʂȐ��̐ێ擙�ɂ������N�������̉t�̐Z�����ω��ɂ���čזE�̑傫���̕ω���������ꂽ�Ƃ��Ă��A���炪�זE�O���̕ω������m���đ傫�������ɂ���悤�ɒ��߂��Ă��܂��B�̉t�����Z������ԂɂȂ�ƁA�זE�͏k��A�̉t�ɑ����܂܂��i�g���E���C�I�����זE���Ɏ�����čזE�̑傫�������̏�Ԃɕ��A���܂��B���̃��J�j�Y���ߐ��זE�e�ϑ���iRVI�j�@�\�Ƃ����܂��B���̋@�\�́A�זE���B��זE���h�~��Z�������m�ɑ傫����������Ă��܂��B����RVI�������炷Na+�����ɁA��I�𐫃J�`�I���`���l�����֗^���邱�Ƃ�20�N�ȏ�O�Ɏ�����iOkada & Hazama 1989 News
Physiol Sci�j�A���̌�Hypertonicity-induced cation channel
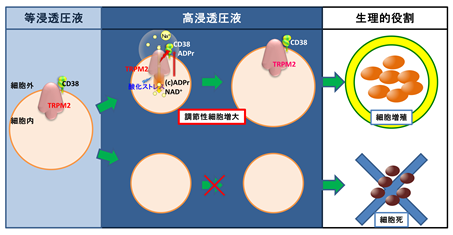
(HICC)�Ɩ�������Ă��܂������A���̕��q���͕̂s���̂܂܂ł���܂����B����A�q�g���זE���ł���HeLa�זE��p���āATRPM2�`���l����C���[�זE��Nudix�̈�ꕔ�����X�v���C�X�o���A���g�iTRPM2∆C�j�����̕��q���̂ł��邱�Ƃ����܂����B����TRPM2�`���l���͔]�A�����A�������A�S���ȂǑ̒��̂��܂��܂Ȋ튯�ɔ������A�����_�f��≷�x�h����T�C�N���b�NADP���{�[�X�Ȃǂɂ���Ċ���������邱�Ƃ��m���Ă���܂������A�{�����ɂ���āA���Z�����h���ɂ����Ă��AHIV��������A�U�^���A�a�A�I�L�V�g�V������ȂǂɊ֗^���镪�q�ł���CD38�i�T�C�N���b�NADP���{�[�X�q�h�����[�[�j�ƌ������đ��ݍ�p�����邱�ƂŁA�����������Ƃ����V���ȋ@�\��������܂����B
�{�������ʂ́A�h�C�c�@�}�b�N�X�v�����N�E���q�����w������ (Frank Wehner����)�Ƌ��s��w�E�n�����w�� (���c���叕���E�X �א� ����)�Ƃ̍��ۓI���������ɂ����̂ł��B
�i�ڍׂ́A�������N���b�N���Ă��������B�j