脳の中で信号を伝える役割をしている神経細胞は、神経細胞と神経細胞の間にシナプスと呼ばれる“つなぎ目”をつくり複雑な神経回路を作っています。シナプス一つ一つの大きさは1ミクロン(マイクロメートル)ほどですが、神経細胞1個あたり1万個にも及ぶシナプスがあり、それが神経細胞内の正しい「場所」で、一定範囲の「数」と「サイズ」で一生涯維持されます。一方、 それら“つなぎ目”(シナプス)の数、サイズ、伝達効率は、経験や刺激の種類に応じて柔軟に変化することも知られています。こうしたシナプスの“精緻性”と“柔軟性”は、脳の発達や高次機能に不可欠であり、そのバランスの破綻が様々な神経系疾患の発症につながります。今回、自然科学研究機構 生理学研究所の深田正紀教授ならびに深田優子准教授の研究グループは、最先端の顕微鏡と新たに開発した蛍光プローブを用いて、生きた神経細胞のシナプスがダイナミックに変化する様子を直接‘視る’ことに成功しました。これによって、シナプスがさらに小さなナノサイズの構造単位(ナノドメイン)が集まってできていることを発見し、脂質修飾酵素DHHC2がその数とサイズを制御していることを明らかにしました。本研究成果は米国の細胞生物学誌(Journal of Cell Biology)に掲載されます(2013年7月8日号)。
研究グループは、脂質修飾酵素DHHC2に注目。この脂質修飾酵素は、神経細胞の中でもシナプスが存在する樹状突起と呼ばれる突起に多く存在しています。この酵素はシナプスの土台となるタンパク質(PSD-95と呼ばれるタンパク質)に脂質(パルミチン酸という脂肪酸の一つ)をくっつけ(脂質修飾)、シナプスの位置を決めます。研究グループは、この酵素によって脂質修飾されたPSD-95を生きた細胞で’視る’ことができるプローブを開発し、最先端の特殊な蛍光顕微鏡(STED超解像顕微鏡)で観察しました。すると、1つ1つのシナプスは、脂質修飾されたPSD-95 からなる更に小さなナノサイズの構造単位(ナノドメイン)が集まってできていることを発見しました。また、シナプスの「数」や「サイズ」は、シナプスに存在するDHHC2の働きによって維持されていることを明らかにしました。さらに、DHHC2は神経の活動に応じてダイナミックにシナプスの「サイズ」を変化させることを明らかにしました。
深田教授は「今回見出した脂質修飾酵素DHHC2は、シナプスを正常に維持することで、脳の働きの原動力となっていると考えられます。今後は、記憶や学習などにおけるDHHC2の役割を明らかにするとともに、DHHC2の機能異常と精神発達遅滞や認知症など脳病態との関連を明らかにすることが必要であると考えます。DHHC2の酵素活性を修飾する薬剤は、脳疾患の魅力的なターゲットとなるかもしれません。」と話しています。
本研究は、ヒューマン・フロンティア・サイエンス・プログラム(HFSPO) (H18-21) (研究代表者深田正紀)による支援の下に、仏国キュリー研究所のフランク・ペレス博士らとの国際共同研究として開始しました。その後、本研究は、最先端・次世代研究開発プログラム(内閣府) (H22-25)(研究代表者深田正紀)による支援を受けて行われました。
1.超解像顕微鏡(STED顕微鏡)と新たに開発した蛍光プローブを用いることにより、これまで知られていなかったシナプスの中のナノサイズのサブドメインを発見しました。
2.脂質修飾酵素DHHC2によって、シナプスが正しい「数」と「サイズ」で維持、再構築されるメカニズムを解明しました。
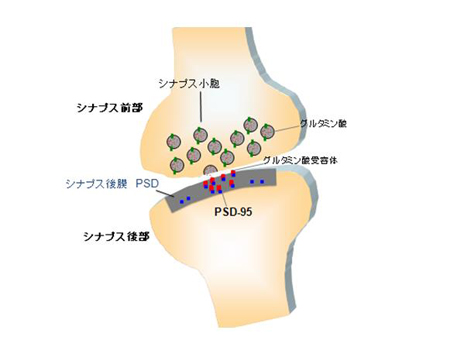
神経と神経の“つなぎ目”であるシナプス。シナプスは、2つの神経細胞(シナプス前部とシナプス後部と書いてある神経細胞)のつなぎ目です。大きさが、約1ミクロン(マイクロメートル)ほどで、髪の毛の太さの100分の1ほどの小さな小さな突起が互いに結合しています。その体積は、1ミリリットルのおおよそ1兆分の1となります。
また、シナプス後部には、シナプス・タンパク質であるPSD-95が土台として存在しています。
このような極めて微小な部分で起きている化学反応は、試験管を用いるような通常の方法で調べることはできません。そこで、その中で起きているダイナミックな変化をのぞくために、最先端の蛍光顕微鏡技術が活躍しています。
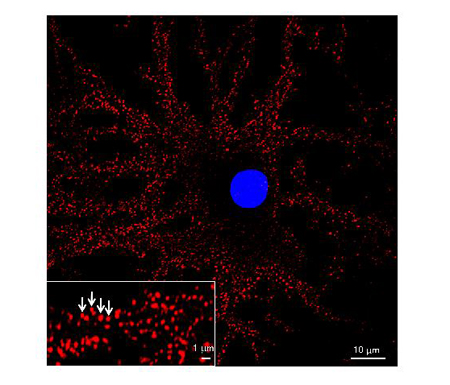
星の数ほどある小さなシナプス(赤い点、直径1マイクロメートル未満)は、一定の範囲でサイズと数が維持されている。いったいどのようにしてシナプスができる場所と数、サイズが決まるのだろう。神経細胞の核(遺伝子情報が貯蔵されている場所、直径10マイクロメートル程度)を青色で示した。左下に拡大図を示した(矢印がひとつひとつのシナプスを示す)。
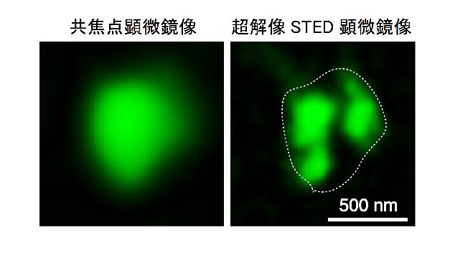
今回、新たに脂質修飾(パルミトイル化)されたシナプス・タンパク質(PSD-95)だけを検出する蛍光プローブを開発し、生きた神経細胞のシナプスを可視化することに成功しました。また、超解像STED顕微鏡(右)を用いることで、従来の共焦点顕微鏡(左)ではひとつのかたまりにしか見えなかったシナプスが、実はナノ単位の幾つかの構造(ナノドメイン)の集まりであることが分かりました。また、一つのナノドメインは平均の直径が約200 ナノメートルであることが分かりました。シナプスは1から4あるいはそれ以上のナノドメインが集まってできていました。
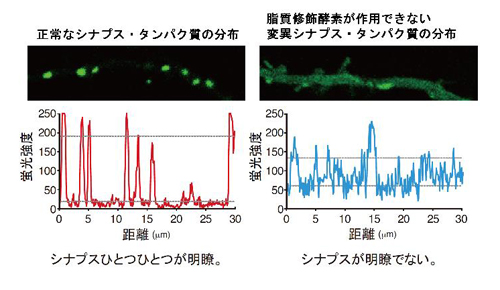
シナプス・タンパク質PSD-95を脂質修飾(パルミトイル化)する酵素のうち、シナプスに存在するDHHC2が機能しないとナノドメインが作られず、しいてはシナプスの「サイズ」や「数」が減少することがわかりました。
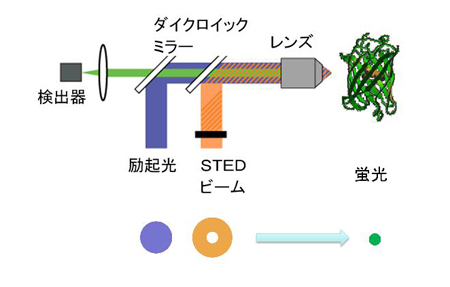
<参考> 超解像顕微鏡 (STED顕微鏡)
STED顕微鏡は、青色の励起光にあわせて、STEDビームとよばれるドーナツ状の長波長の光をあてることにより、中心のごく一部の蛍光を解像度高くとらえる最先端の顕微鏡技術です。
従来の共焦点顕微鏡で撮影した画像に比べるとSTEDによる画像はより高い空間分解能(理論的には80 ナノメートル)を有し、これまで見逃されていた微細構造や動態をより正確に解析することが可能となってきました。
DHHC2の機能異常と精神発達遅滞や認知症など脳病態との関連も
脂質修飾酵素DHHC2によって、神経と神経の“つなぎ目”(シナプス)の数とサイズが精緻にダイナミックに調節されていることがわかったことから、この酵素が正常に機能することが、脳の高次機能に不可欠であると考えられます。今後は、記憶や学習などにおけるDHHC2の役割を明らかにするとともに、DHHC2の機能異常と精神発達遅滞や認知症など脳病態との関連も調べます。DHHC2の酵素活性を修飾する薬剤は、脳疾患の魅力的なターゲットとなるかもしれません。
Local palmitoylation cycles define activity-regulated postsynaptic subdomains
Yuko Fukata, Ariane Dimitrov, Gaelle Boncompain, Ole Vielemeyer, Franck Perez, and Masaki Fukata
米国の細胞生物学誌(Journal of Cell Biology)2013年7月8日発行
<研究に関すること>
自然科学研究機構 生理学研究所 生体膜研究部門 教授
深田 正紀(フカタ マサキ)
〒444-8787 愛知県岡崎市明大寺町字東山5-1
Tel:0564-59-5873 Fax:0564-59-5870
E-mail:mfukata@nips.ac.jp
自然科学研究機構 生理学研究所 生体膜研究部門 准教授
深田 優子(フカタ ユウコ)
〒444-8787 愛知県岡崎市明大寺町字東山5-1
Tel:0564-59-5873 Fax:0564-59-5870
E-mail: yfukata@nips.ac.jp
<広報に関すること>
自然科学研究機構生理学研究所 広報展開推進室
TEL:0564-55-7723 FAX:0564-55-7721
E-mail:pub-adm@nips.ac.jp