慢性疼痛は、「脳が生み出す理不尽な痛み」とも呼ばれる慢性的な痛みのことで、急性期の痛みが過ぎたあとも、三か月以上にわたって引き続くのが特徴です。その長く持続する痛みのため、患者は時に精神的な苦痛も感じ、日常生活に支障をきたすなど、社会的な問題にもなっています。そもそも、この慢性疼痛は、急性期の末梢神経の炎症や損傷がきっかけとなって、脳の中に痛みを長く感じさせるような仕組みが生じるからであると考えられていましたが、脳の中で実際にどのような神経回路の変化が起こっているのかについては解明されていませんでした。今回、自然科学研究機構・生理学研究所の鍋倉淳一教授の研究グループは、慢性疼痛の際には、脳の神経回路が盛んに組み換わってしまうことを証明しました。これによって痛みの感覚が過剰になり長く続く脳内メカニズムを明らかにしました。最先端の二光子レーザー顕微鏡イメージング技術を用いた研究成果です。本発表は、研究グループによって米国神経科学学会誌(ザ・ジャーナル・オブ・ニューロサイエンス)などに掲載された三編の研究成果をまとめたものです。
研究グループは、まず、マウスの脚の神経である坐骨神経が傷ついた神経因性慢性疼痛モデルマウスの脳を用いて実験をしました。このマウスの脳の感覚野と呼ばれる部分を調べたところ、末梢神経傷害による異常な痛み感覚により、感覚野の神経回路をつくる神経と神経のつながり(シナプス)が、神経の傷害後数日以内に劇的に変化し、脳の中の神経回路の組み換えが活発に起こることを明らかにしました。この際、末梢神経の傷害前に存在していたシナプスは減ったり無くなったりしてしまうのに対して、逆に、異常な痛み感覚に応じたシナプスが強くなったり、異常感覚によって新たに作られたシナプスがそのまま残ってしまうことが明らかになりました。さらに、研究グループは、こうした脳の感覚野の神経回路の変化によって、実際に感覚野の神経の活動が活発になることを見出しました。また、脳の感覚野の神経からの過剰な出力を受け、情動などにも関連する前帯状回(ACC)と呼ばれる脳の別の部位の活動も活発となり、これが慢性疼痛を増強していることを明らかにしました。
鍋倉教授は「実際、慢性疼痛を起こしたマウスの感覚野の神経の活動を抑えると、前帯状回(ACC)の活動も抑えられ、マウスの疼痛反応が減ることもわかりました。将来的には、今回発見されたこうした神経回路の変化を狙った新たな慢性疼痛治療戦略をたてることが出来るものと期待されます」と話しています。
本研究は文部科学省・科学研究費補助金による支援をうけて行われました。
1.最先端の二光子レーザー顕微鏡による観察により、慢性疼痛モデルマウスの脳では、末梢神経の傷害後の慢性疼痛の発達期(1週間以内)に、脳の中で神経回路の組み換えが活発に起きることがわかりました(文献1、文献3)。
2.末梢神経の傷害前に存在していたシナプスは減ったり無くなったりしてしまうのに対して、逆に異常な痛み感覚に応じたシナプスが強くなったり、異常感覚によって新たに作られたシナプスがそのまま残ってしまうことが分かりました(文献1)。
3.さらに、慢性疼痛にともなって、感覚野の神経の活動が活発になり、情動などにも関連する前帯状回(ACC)と呼ばれる脳の部位の活動も活発となることが分かりました(文献2)。
慢性疼痛が生まれる際には神経回路の組み換えが活発に起きる
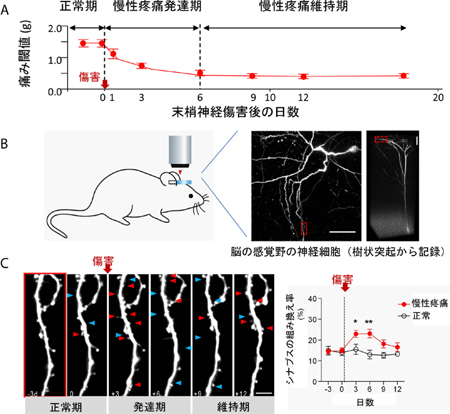
(A) 末梢神経の傷害のあと、日数を追うとともに、痛みに対する感受性(痛み閾値)が過敏になり、1週間をすぎたところから、ちょっとした刺激でも痛みを覚えるようになります。ここでは荷重(g)刺激によって痛み反応を引き起こしました。
(B) 慢性疼痛モデルマウスの脳(感覚野)の中の神経回路の様子を、最先端の二光子レーザー顕微鏡で観察しました。脳(感覚野)の大脳皮質錐体神経細胞の樹状突起から記録しました。
(C) 神経と神経のつながりであるシナプスを観察したところ、末梢神経傷害の後、慢性疼痛の発達期(1週間以内)には盛んに神経回路の組み換えが起きていることがわかりました。赤矢尻は新しくできたシナプス、青矢尻は無くなったシナプスです。慢性疼痛が確立されると(慢性疼痛の維持期、受傷後1週間以降)、こうした神経回路の組み換えの頻度は下がります。
異常感覚によって新たなシナプスが盛んに作られる
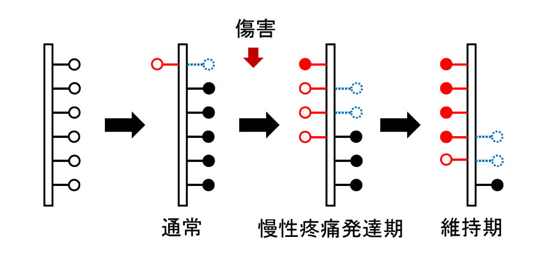
神経細胞のシナプスの組み換えの様子(模式図)。慢性疼痛の発達期では、通常に比べて盛んに神経の組み換えがおこり、古いシナプスがなくなり、異常感覚に応じた新しいシナプスが盛んに作られていました。慢性疼痛維持期では、こうした異常感覚に応じた新しいシナプスが残存してしまうことがわかりました。赤は新しく作られたシナプス、青は無くなったシナプスを表しています。
慢性疼痛では脳の神経細胞の痛み応答も増加している
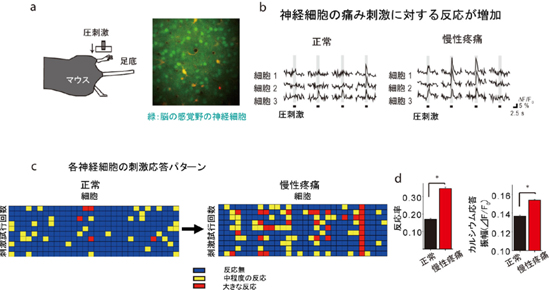
(a) 二光子レーザー顕微鏡によるカルシウム・イメージング技術を適用し、慢性疼痛モデルマウスの痛み刺激(圧刺激)に対する脳(感覚野)の神経細胞の活動(カルシウム応答)を記録しました。
(b) 正常なマウスでは反応しないくらいの圧刺激でも、慢性疼痛モデルマウスの神経細胞では大きく反応することがわかりました。
(c) 脳の30個の神経細胞の痛みに対する反応を記録(10回刺激)。慢性疼痛モデルマウスでは正常よりも大きな反応を示す細胞が多数みられました。
(d) (c)の結果を平均した棒グラフ。痛み反応の増加とともに、神経細胞の刺激に対する反応性と神経細胞の応答(カルシウム応答)も増加していました。
慢性疼痛発生の神経回路モデル
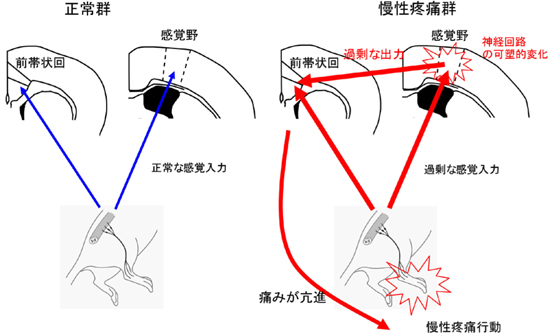
研究グループによる今回の三編の研究成果より、以下のようなモデルが考えられます。慢性疼痛の発達期には、神経回路の組み換えが盛んにおこります。これによって、神経回路が組み換わり、脳の感覚野の神経細胞が痛み刺激に対して過剰に反応するようになってしまいます。また、この感覚野の神経細胞の過剰な痛み反応が脳の情動をつかさどる前帯状回に出力されるようになり(図右)、これによって、痛み感覚が増強し、慢性疼痛行動を生みだすものと考えられました。実際、感覚野の神経細胞の活動を薬によって抑えると、前帯状回の活動も抑えられ、慢性疼痛行動が減ることがわかりました。
慢性疼痛を引き起こす脳内メカニズムの解明へ
今回の研究成果により、慢性疼痛の際には、脳の神経回路が組み換わってしまっていることがわかりました。とくに、脳の感覚野の神経細胞の過剰な痛み反応が前帯状回に伝わることで慢性疼痛の痛み感覚の増強を引き起こしていることがわかりました。こうした神経回路の可塑的な変化に着目した新たな慢性疼痛治療戦略の構築ができるものと期待されます。
本発表は、研究グループにより今年度に発表された三編の研究成果をまとめたものです。
文献1.Rapid synaptic remodeling in the adult somatosensory cortex following peripheral nerve injury and its association with neuropathic pain.
Kim SK, Nabekura J.
米国神経科学会雑誌(ザ・ジャーナル・オブ・ニューロサイエンス)
J Neurosci. 2011 Apr 6;31(14):5477-82.
文献2.Inter-regional contribution of enhanced activity of the primary somatosensory cortex to the anterior cingulate cortex accelerates chronic pain behavior.
Eto K, Wake H, Watanabe M, Ishibashi H, Noda M, Yanagawa Y, Nabekura J.
米国神経科学会雑誌(ザ・ジャーナル・オブ・ニューロサイエンス)
J Neurosci. 2011 May 25;31(21):7631-6.
文献3.Phase-specific plasticity of synaptic structures in the somatosensory cortex of living mice during neuropathic pain.
Kim SK, Kato G, Ishikawa T, Nabekura J.
痛みの分子生物学誌(モレキュラー・ペイン)
Mol Pain. 2011 Nov 9;7:87.
<研究に関すること>
鍋倉 淳一(ナベクラ ジュンイチ)
自然科学研究機構 生理学研究所 教授
〒444-8585 岡崎市明大寺町字西郷中38
Tel:0564-55-7851 Fax:0564-55-7853
E-mail:nabekura@nips.ac.jp
<広報に関すること>
小泉 周 (コイズミ アマネ)
自然科学研究機構 生理学研究所 広報展開推進室 准教授
TEL:0564-55-7722、FAX:0564-55-7721
E-mail:pub-adm@nips.ac.jp