てんかん関連リガンド-受容体LGI1-ADAM22によるAMPA受容体制御機構
[背景]
AMPA型グルタミン酸受容体の動態制御機構は、長期増強(LTP)などのシナプス可塑性の根幹をなすものと考えられ、多くの研究者により様々なモデルが提唱されてきました。ごく最近では、LTPの本態は、“シナプス外細胞膜に存在するAMPA受容体のシナプス後膜(PSD)への移動、およびPSDでのAMPA受容体の捕捉効率の上昇である”というモデルが提唱されています。すなわち、PSDにおけるPSD-95の数や機能を制御する分子機構は、シナプス可塑性の根幹を支えるものと期待されます。
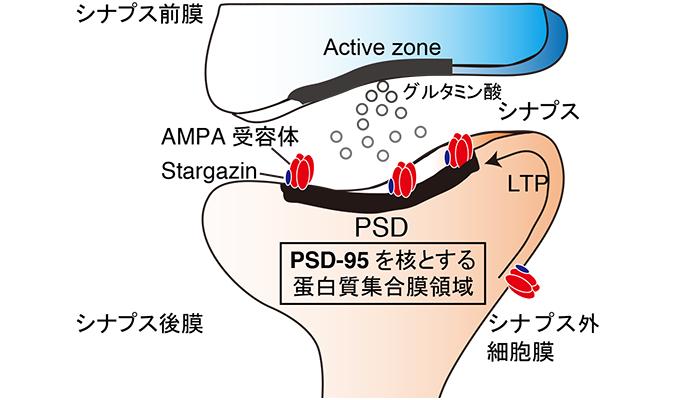
図1 足場蛋白質PSD-95は、AMPA受容体をPSDで捕捉する場(スロット)を提供する。また、PSD-95はPSD構築においても中核的な役割を担う。
[当研究室における研究の経緯]
1) LGI1-ADAM22リガンド、受容体の同定 2006年に我々は、PSD-95を核とする蛋白質複合体をラット脳から精製し、その主要構成成分としてLGI1、ADAM22、およびStargazinを見出しました。LGI1は2002年に3つの独立したグループからヒトの家族性側頭葉てんかんの原因遺伝子として報告された機能未知の蛋白質でした。我々は、分泌蛋白質LGI1が膜蛋白質ADAM22のリガンドとして機能し、AMPA受容体機能を促進することを報告しました。
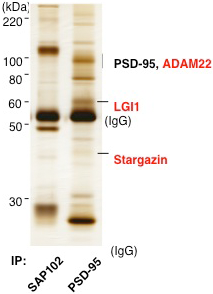
図2 ラット脳からPSD-95を含む蛋白質複合体を精製し、主要構成成分を同定しました。
2) LGI1欠損マウスは致死性てんかんを必発する LGI1ノックアウト(KO)マウスを樹立したところ、全てのマウスは生後3週間以内に致死性てんかんを必発しました。また、LGI1 KOマウスの海馬神経細胞においては、AMPA受容体機能が低下していることを見出しました。Transgenic rescue実験により、LGI1欠損による“てんかん”が単一遺伝子疾患であることを示しました。
3) LGI1に対する自己抗体はLGI1-ADAM22結合を阻害し、辺縁系脳炎を引き起こす 亜急性に近時記憶障害や痙攣、見当識障害をきたす重篤な脳疾患として、辺縁系脳炎という疾患があります。我々は、LGI1に対する自己抗体価と辺縁系脳炎発症との間に極めて高い(ほぼ1対1)相関性があることを見出しました。また、LGI1自己抗体は、LGI1-ADAM22の結合を阻害し、シナプスにおけるAMPA受容体量を減少させることを明らかにしました。
4) LGI1変異は蛋白質の構造異常を引き起こし、てんかんを惹起する 我々は、ヒトのてんかん患者で見られる全てのLGI1変異を体系的に解析し、それらを分泌型、および分泌不全型の2種類の型に分類しました。それぞれのマウスモデルを樹立し解析したところ、分泌型LGI1変異はADAM22との結合能を失っていること、分泌不全型LGI1は蛋白質の構造異常のため細胞内で分解されていることを見出しました。また、ある種の化学シャペロンがマウスモデルのてんかん感受性を改善させることを見出しました。
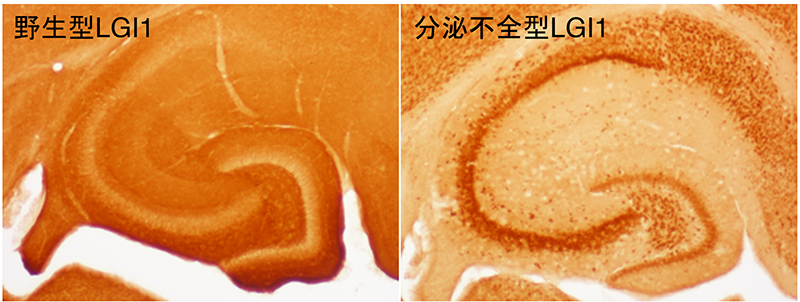
図3 分泌不全型LGI1はシナプスへ輸送されず、細胞体に貯留します(右)。その結果、LGI1-ADAM22によるシナプス伝達の制御が破綻し、てんかん病態が惹起されます。
5) LGI1はPSD-95機能を制御し、シナプスを成熟させる LGI1 KOマウスでは、「PSD-95のAMPA受容体機能を制御する活性(scaffolding activity)」が消失することが明らかになりました。また、ADAM22 KOマウスにおいてもAMPA受容体を介したシナプス伝達が減弱することが明らかとなりました。
6) 今後の展開 a) LGI1-ADAM22によるAMPA受容体制御機構の解明 b) 記憶学習におけるLGI1-ADAM22の役割の解明 c) LGI1-ADAM22が関わるてんかん回路の同定 d) LGI1-ADAM22複合体の構造基盤の解明 e) LGI1分子プローブ、LGI1模倣薬の開発
[研究の意義、波及効果]
ヒトにおける“てんかん”の有病率は歴史を通じて常に約1%程度と報告されています。時に激しいけいれんや意識消失を起こし、社会生活の制限を余儀なくされる為、治療が困難な患者さんもいらっしゃいます。このLGI1-ADAM22は、従来のイオンチャネルを標的とした抗てんかん薬とは異なる新たな創薬の標的になるかもしれません。LGI1によるシナプス制御機構は基礎研究にとどまらず臨床面からもますます注目されているところです。
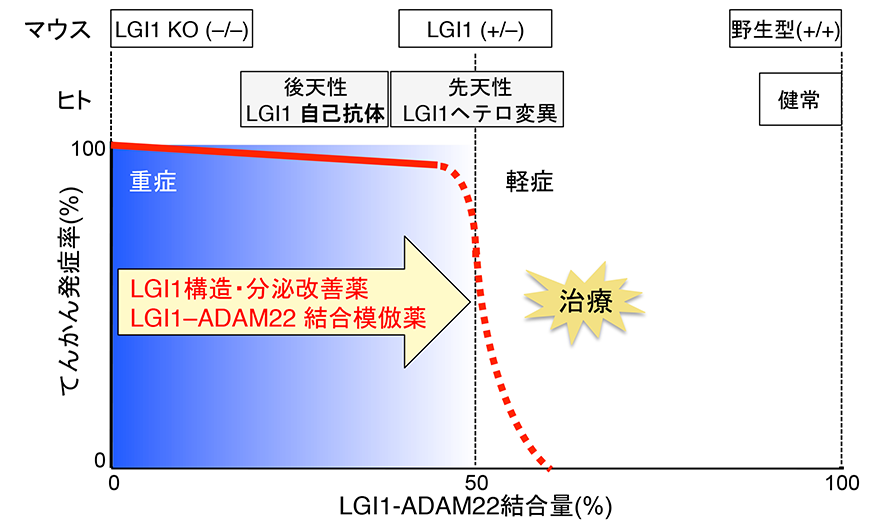
図4 LGI1–ADAM22結合量がある閾値を下回ると“てんかん病態”が生じることが分かってきました。化学シャペロンを代表とする“LGI1構造・分泌改善薬”や“LGI1–ADAM22結合模倣薬”はLGI1の抗てんかん作用を賦活(活性化)することで、新規の抗てんかん薬となることが期待されます。
*私たちは誰しもが納得できる「脳のシナプス伝達の基本原理」の発見を目指すべく、あらゆる手法を用いて直面する課題に挑戦、探究していきます。 Why don’t you join us?