| 唐辛子に含まれるカプサイシンが辛さ(痛み)を生じさせるメカニズムに、感覚神経にあるTRPV1(トリップ・ブイワン)というイオンチャネルの活性化が関与することは、10年以上前から広く知られています。またTRPV1と同じ感覚神経に発現しているアノクタミン1というイオンチャネルが、TRPV1とは独立して痛みを発生させることも知られています。今回、自然科学研究機構 生理学研究所(岡崎統合バイオサイエンスセンター)の高山靖規特任助教、富永真琴教授、古江秀昌准教授は、富山大学の歌大介助教との共同研究により、カプサイシンによってTRPV1が活性化すると、アノクタミン1の活性化が強く誘発され、痛みがさらに増強することを、マウスを用いた研究によって明らかにしました。また今回の研究成果では、アノクタミン1活性の薬剤による阻害が、疼痛の緩和効果を発揮することも証明しました。本研究成果は、米国科学アカデミー紀要(4月7日電子版)に掲載されます。 |
研究グループが注目したのは、マウスの感覚神経に存在するTRPV1と、アノクタミン1という、2つのイオンチャネルです。今回の研究成果では、① TRPV1の活性化に伴い、アノクタミン1が活性化されること、② TRPV1とアノクタミン1の連続したイオンチャネル活性化が、カプサイシンによる痛みをさらに強くさせていること、この2点を発見しました。
カプサイシンによって感覚神経にあるTRPV1が活性化すると、神経が興奮し焼けるような痛み(灼熱痛)が引き起こされます。熱湯などによってもTRPV1は活性化しますが、カプサイシンの作用はより強力です。TRPV1は、ナトリウムイオンやカルシウムイオンなどの陽イオンを通すイオンチャネルですが、カプサイシンによる灼熱痛の原因は、神経細胞外から細胞内へ入ってきたナトリウムイオンの作用によるものであると、これまでは信じられてきました(図1左)。しかし今回の研究によって、TRPV1を介して細胞内に入ってきたカルシウムイオンが、アノクタミン1という別のチャネルの活性化を誘発し、細胞内の塩素イオンが細胞外に放出される結果、神経興奮が増強されて灼熱痛が生じる、という新たなメカニズムを明らかにしました。しかも、TRPV1とアノクタミン1は物理的に結合しており、両者間の距離は理論上20 nm以下と非常に近いことが判明しました(図1右)。
また、マウスの足にカプサイシンを投与した時に観察される痛み行動(足舐め行動)は、アノクタミン1阻害剤によって抑制されました(図2)。さらにアノクタミン1阻害剤は、感覚神経から脊髄の中で、別の神経細胞に痛み信号が伝わる程度も減少させることが判明しました(図3)。
すなわち、TRPV1が強力に活性化された時の痛みには、アノクタミン1の阻害剤が有効であると考えられます。
本研究は文部科学省科学研究費補助金の補助を受けて行われました。
1. TRPV1(トリップ・ブイワン)
唐辛子の辛み成分カプサイシンの受容体(センサー)。感覚神経にあり、カプサイシン、43度以上の熱刺激、酸など複数の痛み刺激で活性化します。TRPV1は陽イオンを通すチャネルで、活性化することによって細胞外から陽イオンが細胞内に流れ込むと、細胞の膜を隔てた電位差(膜電位)がプラスの方向に変化し、感覚神経が発火(興奮)します。その信号が脳に伝わることで、私たちは「痛い(辛い、熱い)」と感じることができます。
2. アノクタミン1
細胞内のカルシウムイオン濃度の増加を感知して開き、塩素イオンなどの陰イオンを通すチャネル。中枢神経では細胞内の塩素イオン濃度が低いため、塩素イオンチャネルが開くと塩素イオンは細胞外から細胞内に流れ込み、膜電位がマイナス方向に変化し、神経細胞の興奮性は抑えられます。これが、麻酔薬や睡眠導入薬の作用メカニズムの一つです。しかし感覚神経では、細胞内の塩素イオン濃度が高いため、塩素イオンチャネルが開くと塩素イオンは細胞内から細胞外に流れ出てしまい、膜電位はプラスの方向に変化し、程度が大きいと発火(興奮)します。
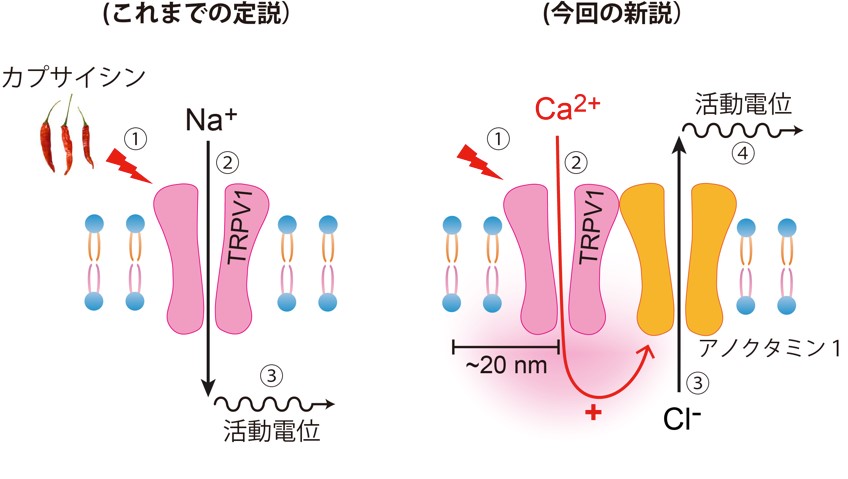 今までは、 ① カプサイシンがTRPV1に作用する、② TRPV1活性化により細胞内にナトリウムイオン(陽イオン)が入る、 ③ 活動電位が発生する(神経が興奮する)、というのが定説でした。これは間違いではありません。しかし、今回の研究から新たにわかったことは、① カプサイシンがTRPV1に作用する、② TRPV1活性化によりカルシウムイオンが細胞内に入り半径20 nm以内にあるアノクタミン1がカルシウムイオンによって活性化する、③ 感覚神経では細胞内塩素イオン濃度が高いので、塩素イオン(陰イオン)が細胞外に出る、④ 活動電位が発生する、というものです。
今までは、 ① カプサイシンがTRPV1に作用する、② TRPV1活性化により細胞内にナトリウムイオン(陽イオン)が入る、 ③ 活動電位が発生する(神経が興奮する)、というのが定説でした。これは間違いではありません。しかし、今回の研究から新たにわかったことは、① カプサイシンがTRPV1に作用する、② TRPV1活性化によりカルシウムイオンが細胞内に入り半径20 nm以内にあるアノクタミン1がカルシウムイオンによって活性化する、③ 感覚神経では細胞内塩素イオン濃度が高いので、塩素イオン(陰イオン)が細胞外に出る、④ 活動電位が発生する、というものです。
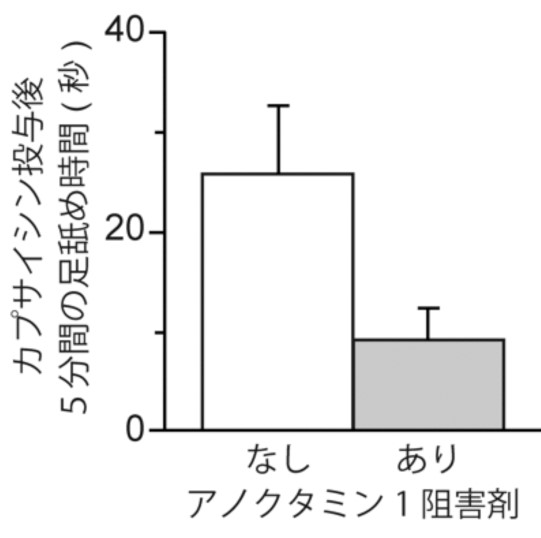
カプサイシンを足に投与するとマウスはしばらく舐め続けます。この足舐め時間の長さで痛みの程度を評価します。図2は、カプサイシン投与後5分間における足舐め時間の合計です。アノクタミン1阻害剤の同時投与により足舐め行動(痛み関連行動)が有意に抑制されました。
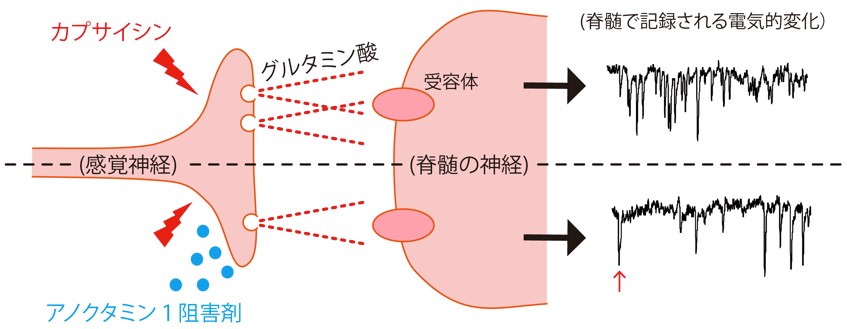
痛みの信号は、脊髄でシナプスという構造において神経伝達物質(グルタミン酸)によって次の神経に伝達されます。そして、痛み信号は脳へと伝わっていきます。この伝達は電気的変化を伴い、1回の伝達は1個の波(電気信号)(図3右、赤矢印)として観察することができます。図に示すように、カプサイシンが感覚神経に作用すると脊髄の神経において多くの波が観察されます。アノクタミン1阻害剤を同時投与するとその数が減っていることがわかります。すなわち、図2のように手先や足先のような感覚神経終末で発生する痛み信号だけでなく、神経伝達の過程で生じるTRPV1関連の痛み信号の抑制にもアノクタミン1阻害が有効であると考えられます。
鎮痛作用のある新しい合成薬や生薬、人工タンパク質の開発
TRPV1を標的とした鎮痛薬は、作用が弱い上に体温上昇を引き起こしてしまうので、臨床試験をクリアした薬剤はありません。TRPV1とアノクタミン1の複合体を標的とした薬剤開発は、とても期待されています。またアノクタミン1は、ワインや緑茶に含まれるタンニン酸によって阻害されることが知られています。タンニン酸以外にも、普段私たちが口にしているものの中に、アノクタミン1を標的として痛みを抑える成分がある可能性は大きく、その発見が期待されます。さらに、TRPV1とアノクタミン1は非常に近い位置関係で相互作用しています。細胞内には数多くのカルシウム結合性タンパク質があるので、両者間の距離が離れれば離れるほど相互作用は起こりにくいと考えられます。TRPV1とアノクタミン1の間に割って入り、両者を引き離すようなタンパク質を開発することができれば、これは全く新しい鎮痛薬になると考えられます。
つまり本研究成果は、新しい鎮痛薬や疼痛治療法開発の一助となる研究と言えます。
Pain-enhancing mechanism through interaction between TRPV1 and anoctamin 1 in sensory neurons.
Yasunori Takayama, Daisuke Uta, Hidemasa Furue, Makoto Tominaga.Proceedings of the National Academy of Sciences, USA. 2015年4月7日
<研究について>
自然科学研究機構 生理学研究所 細胞生理研究部門
教授 富永真琴 (とみなが まこと)
<広報に関すること>
自然科学研究機構 生理学研究所 研究力強化戦略室
生理学研究所・研究力強化戦略室