「てんかん」は人口の約1%という高い発症率を示す脳神経疾患で、その病態の解析は、病気の予防、進行の防止、治療方法の開発の上で極めて重要である。本研究においては、その病態解析を目的として、持続てんかん発作モデルであるカイニン酸けいれん重積状態を示すラット脳内の分子変化を生化学的・免疫組織学的に解析した。蛋白質リン酸化酵素「ERK1/2(Extracellular signal-regulated kinase 1/2)」は、神経活動の興奮性が増大する際に、脳内でその活性が増加することが知られている。しかしながら、その活性化に伴って、情報伝達先となる基質蛋白質のリン酸化が同様に上昇しているのかどうかを調べた研究はわずかしかない。我々はこれまで様々なけんれんモデルを用いて、ERK1/2活性とシナプス前に存在するERK1/2の基質である「シナプシンI」のリン酸化との関連を調べ、生体内においてもシナプシンIのリン酸化がERK1/2活性によって実際に制御されていることを示してきた。
本研究において、カイニン酸誘発けいれん重積状態のラット脳を解析したところ、ERK1/2の顕著な活性化が観察される一方で、これと対照的に、その基質蛋白であるシナプシンIのリン酸化は大きく減少していた(図A)。これら変化はけいれん中に限られており、けいれんから回復した後にはすべて消失していた。この結果は、持続てんかん発作活動時には、ERK1/2の活性化とシナプシンIの脱リン酸化という一見相反する現象が起こることを示すものである。このことは、生体内における基質蛋白のリン酸化状態がリン酸化酵素であるキナーゼのみならず、脱リン酸化酵素であるフォスファターゼとの活性バランスによって制御されていることを示している(図B)。このように神経活動の興奮性の増大時に、ERK1/2の顕著な活性化にもかかわらず、シナプシンIの脱リン酸化が起こるような場合は(図B、右端)、けいれん活動が終息した後に不可逆的な結果がもたらされる可能性を示すのかもしれない。
Yoko Yamagata and Angus C. Nairn
Contrasting features of ERK1/2 activity and synapsin I phosphorylation at the ERK1/2-dependent site in the rat brain in status epilepticus induced by kainic acid in vivo.
Brain Research, 1625: 314-323, 2015
doi: 10.1016/j.brainres.2015.08.023
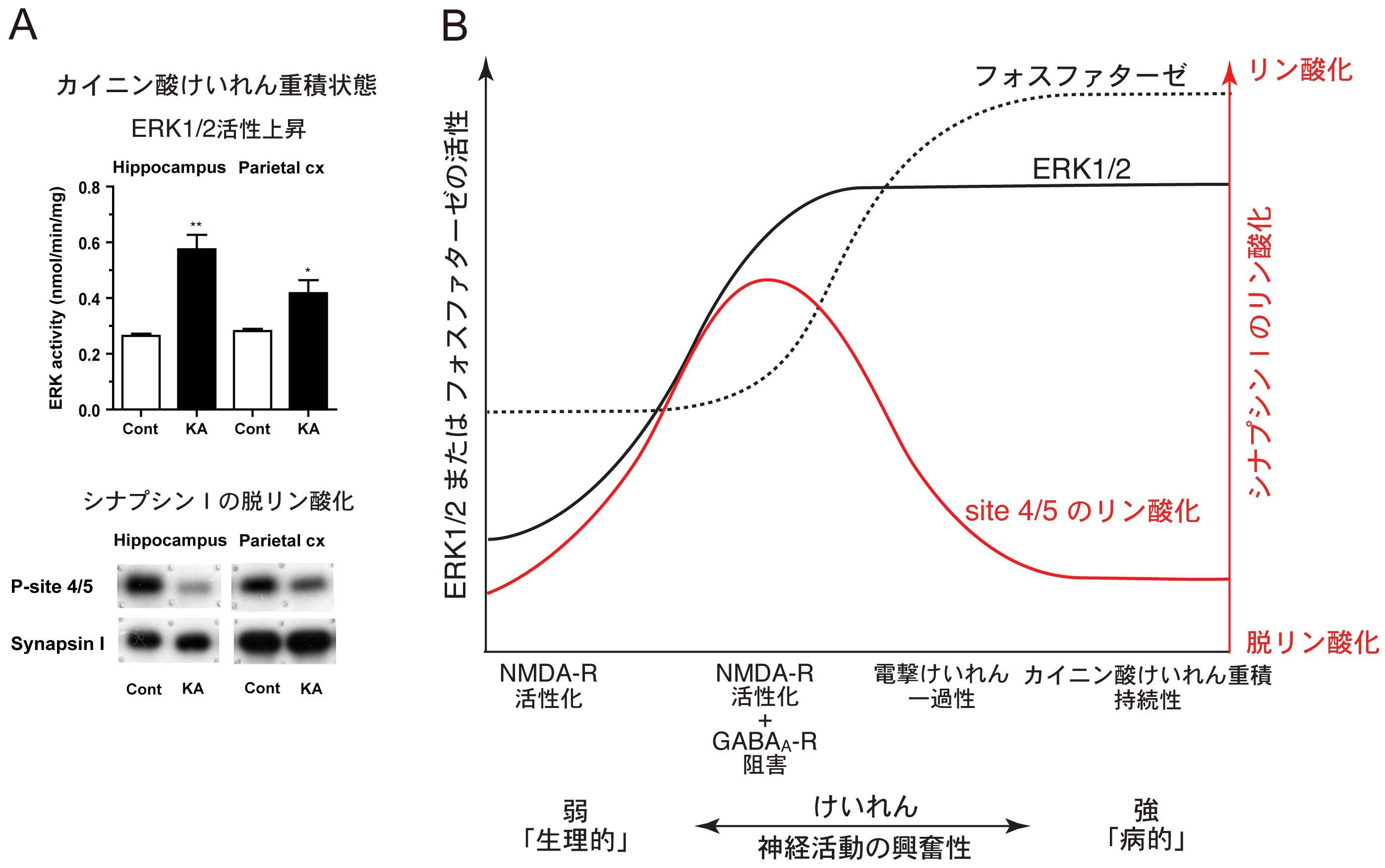
A:カイニン酸けいれん重積状態では、脳内においてERK1/2の顕著な活性上昇が認められたが、ERK1/2によるシナプシンIのsite 4/5のリン酸化は逆に大きく低下していた。
B:これまでの研究結果(Yamagata et al., 2002, 2013)と合わせると、生体内におけるシナプシンIのリン酸化は、神経活動の興奮性の増大に従って、ERK1/2とフォスファターゼ(おそらくはカルシニューリン)の活性のバランスによって動的に制御されているものと考えられる。(1)けいれん活動が比較的弱いときには(左端)、フォスファターゼの活性が上昇するがERK1/2の活性は上昇せず、シナプシンIの脱リン酸化が起こる。(2)けいれん活動が中等度となると(中央左)、ERK1/2活性の上昇がフォスファターゼ活性の上昇を上回り、シナプシンIのリン酸化が上昇する。(3)けいれん活動がある程度強いが一過性である場合には(中央右)、フォスファターゼとERK1/2は共に活性が上昇するものの、フォスファターゼの活性上昇が先行するため、けいれん中にはシナプシンIの脱リン酸が優位に観察される。(4)けいれん活動がさらに強度かつ持続的となると(右端)、フォスファターゼ活性の上昇がERK1/2活性の上昇を上回り、その結果シナプシンIの強い脱リン酸化が起こる。カイニン酸けいれん重積状態はこれに相当する。