|
名古屋大学医学部附属病院 糖尿病・内分泌内科の宮田 崇 医員(筆頭著者)、萩原 大輔 病院講師(責任著者)、同大医学系研究科 糖尿病・内分泌内科学の有馬 寛 教授(責任著者)、自然科学研究機構 生理学研究所 生体機能調節研究領域 超微形態研究部門および自治医科大学医学部 解剖学講座組織学部門の大野 伸彦 教授、岡山大学大学院自然科学研究科 理学部附属臨海実験所の坂本 浩隆 准教授らの研究グループは、家族性中枢性尿崩症*1モデルマウスを用いて、小胞体*2における新たな異常タンパク処理メカニズムを明らかにしました。 小胞体ストレス*3は、糖尿病や神経変性疾患を始めとした多くの病気に関係していることが分かっています。小胞体に蓄積した異常タンパクに対する処理メカニズムとしてユビキチン-プロテアソーム系*4あるいはオートファジー*5が広く知られていますが、いずれにおいても異常タンパクを小胞体から細胞質へ輸送あるいは隔離した後に分解が行われます。一方で、小胞体内で凝集体を形成し、輸送隔離されることができなくなった異常タンパクがどのようなメカニズムで処理されるかは明らかになっていませんでした。今回研究グループが解析を行った家族性中枢性尿崩症のモデルマウスでは脳内に存在するバソプレシンニューロン*6の小胞体の一部に異常タンパクの凝集体が隔離された区画(ER-associated compartment: ERAC)が形成されることが分かっており、本研究ではERAC内の異常タンパク凝集体の分解機構の解明を目指しました。 連続ブロック表面走査電子顕微鏡*7を用いた解析により、ERACが正常小胞体とつながっていることが示されたとともに、ERACへのライソソーム*8の融合が明らかとなりました。また免疫電子顕微鏡*9による解析ではERAC内にライソソーム関連分子が発現しており、さらには薬理学的解析によりERAC内の凝集体はライソソームによる分解を受けていることが示されました。以上の結果は、異常タンパク凝集体が小胞体から細胞質へ輸送隔離されることなく小胞体内部でライソソームにより分解されることを意味しており、新たな異常タンパク処理メカニズムの存在が明らかとなりました。 今後、このメカニズムをさらに詳しく解明していくことで、小胞体ストレスに関連する多くの疾患に有効な治療薬の開発に繋がる可能性があります。 本研究は、米国Cell Pressより発行されている科学誌「iScience」(2020 年10月7日付(米国東部時間)の電子版)に掲載されました。 |
○小胞体に異常タンパクが蓄積することによって生じる小胞体ストレスは、糖尿病や各種神経変性疾患を含めた多くの疾患の病態に関与している。
○小胞体に蓄積した異常タンパクは、ユビキチン-プロテアソーム系あるいはオートファジーによって分解されることが知られているが、いずれも異常タンパクを小胞体から細胞質へ輸送あるいは隔離した後に分解が行われる。
○本研究の結果、小胞体内で凝集体を形成した異常タンパクを小胞体から輸送隔離することなく小胞体内部でライソソームにより分解する、新規の異常タンパク処理機構が存在することが示された。
○この新たな分解メカニズムに関してより詳細な分子の仕組みの解明を進めることで、小胞体ストレスに関連する多くの疾患に有効な治療薬の開発に繋がる可能性がある。
小胞体はタンパク質の折りたたみを担う細胞内小器官です。一方で、種々の要因により正常な構造に折りたたまれなかった異常タンパクが小胞体に蓄積すると小胞体ストレスが生じます。小胞体ストレスに対する生体の防御機構(小胞体ストレス応答)として、小胞体に蓄積した異常タンパクを処理するためユビキチン-プロテアソーム系あるいはオートファジーが誘導されること知られており、これらの機構では異常タンパクは小胞体から細胞質へ輸送あるいは隔離した後に分解されます。
家族性中枢性尿崩症は生後数ヶ月から数年で緩やかに進行する尿崩症症状が現れる遺伝性疾患であり、バソプレシンニューロンの小胞体に異常タンパクが蓄積することによる小胞体ストレスが病態の主体であることが知られています。本研究グループは過去に家族性中枢性尿崩症モデルマウスを作り出し、バソプレシンニューロンの小胞体の一部に異常タンパクの凝集体が隔離された区画(ER-associated compartment: ERAC)が形成されることを発見しました。しかしながら、ERAC内の異常タンパクは凝集体を形成していることから小胞体から細胞質へ輸送隔離することが困難と考えられ、ユビキチン-プロテアソーム系あるいはオートファジーといった従来の異常タンパク処理メカニズムとは異なる別の分解メカニズムが存在する可能性があり、本研究ではその解明を目指しました。
家族性中枢性尿崩症モデルマウスにおいて連続ブロック表面走査電子顕微鏡を用いてバソプレシンニューロンにおけるERACの詳細な形態の解析を実施したところ、ERACと正常小胞体との連続性が確認され(図1)、またERACへのライソソームの融合が観察されました(図2)。ライソソーム関連分子に対する抗体を用いた免疫電顕を施行したところ、ライソソーム関連分子がERACの内部に存在していることが分かりました。さらには、家族性中枢性尿崩症モデルマウスにオートファジー誘導薬のラパマイシンを投与したところERACの数は有意に減少していた一方で、ライソソーム阻害薬のクロロキンを投与したところERACの数は有意に増加しており、ERAC内の凝集体はライソソームによる分解を受けていることが示されました。
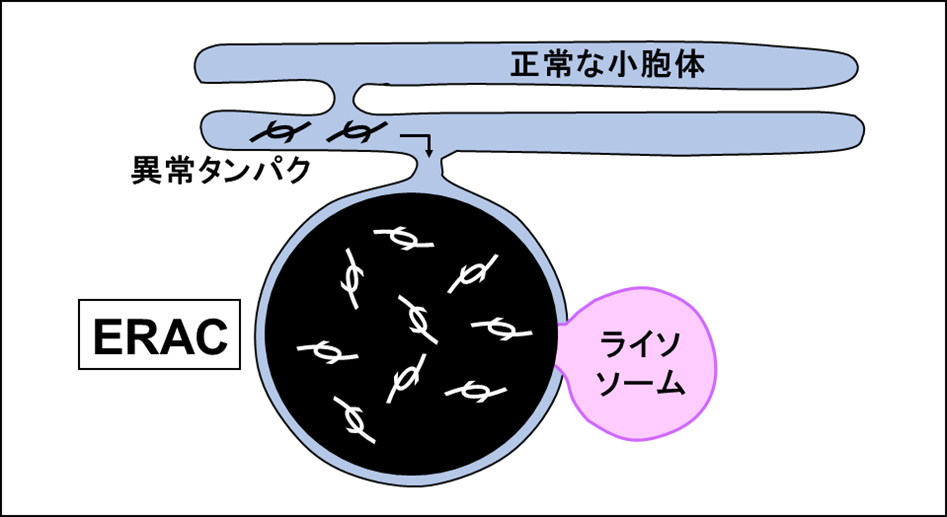
以上の結果から、小胞体内に蓄積した異常タンパク凝集体は小胞体から細胞質へ輸送隔離されることなく小胞体内部で分解されていることが明らかとなりました。今回発見したこの分解メカニズムは従来のユビキチン-プロテアソーム系あるいはオートファジーとは異なる、新たな異常タンパク処理メカニズムです(図3)。
小胞体ストレスが病態に関与する他の病気の動物モデルでも家族性中枢性尿崩症モデルマウスと同様にERACの形成が報告されており、小胞体ストレスが生じうる体中のいろいろな細胞においてERACの形成は普遍的な小胞体ストレス応答であると考えられます。今後、本研究で示された新たな異常タンパク処理メカニズムに関してより詳細な分子の仕組みが解明されれば、小胞体ストレスが病態形成に関与する多くの疾患に共通の仕組みが解明される可能性があり、さらにはこれらの疾患に対する新たな治療薬の開発に繋がることも期待されます。
図1 図2

図3
※1 家族性中枢性尿崩症:生後数ヶ月から数年で緩やかに進行する尿崩症症状(多尿、多飲など)が現れる遺伝性疾患。
※2 小胞体:新たに合成されたタンパク質の折りたたみを担う細胞内小器官。
※3 小胞体ストレス:適切に折りたたまれなかった異常タンパクが小胞体に蓄積した状態。
※4 ユビキチン-プロテアソーム系:細胞質の異常タンパクをユビキチン化してプロテアソームで分解する、主要な細胞内分解系の一つ。
※5 オートファジー:異常タンパクや傷ついた細胞内小器官を隔離膜で隔離してオートファゴソームを形成しライソソームが融合することで分解する、主要な細胞内分解系の一つ。
※6 バソプレシンニューロン:バソプレシンは抗利尿ホルモンとも呼ばれ、視床下部に存在するバソプレシンニューロンで合成され、 ニューロンの末端である下垂体後葉から血液中に分泌される。血液中のバソプレシンは、腎臓に働いて水の再吸収を増加させる働きをする。
※7 連続ブロック表面走査電子顕微鏡:組み込み式ミクロトームによる表面切削と走査電子顕微鏡による試料の断面観察を交互に反復することにより、数百m2以上に及ぶ比較的広範囲の領域からの連続切片画像を数nm程度の解像度で迅速に取得できる
※8 ライソソーム:内部に加水分解酵素を含み、消化分解作用をもつ細胞内小器官。
※9 免疫電子顕微鏡:目的とするタンパク質の局在を、抗原抗体反応を利用して電子顕微鏡下で検出する方法。
掲雑誌名:iScience
論文タイトル:Degradation of mutant protein aggregates within the endoplasmic reticulum of vasopressin neurons
著者:Takashi Miyata1, Daisuke Hagiwara1,*, Yuichi Hodai1, Tsutomu Miwata1, Yohei Kawaguchi1, Junki Kurimoto1, Hajime Ozaki1, Kazuki Mitsumoto1, Hiroshi Takagi1, Hidetaka Suga1, Tomoko Kobayashi1, Mariko Sugiyama1, Takeshi Onoue1, Yoshihiro Ito1, Shintaro Iwama1, Ryoichi Banno1,2, Mami Matsumoto3, Natsuko Kawakami4, Nobuhiko Ohno5,6, Hirotaka Sakamoto4, and Hiroshi Arima1,*
*Corresponding author
所属:1 Department of Endocrinology and Diabetes, Nagoya University Graduate School of Medicine, 65 Tsurumai-cho, Showa-ku, Nagoya, 466-8550, Japan
2 Research Center of Health, Physical Fitness and Sports, Nagoya University, Nagoya, 464-8601, Japan
3 Section of Electron Microscopy, Supportive Center for Brain Research, National Institute for Physiological Sciences, Okazaki, 444-8787, Japan
4 Ushimado Marine Institute, Graduate School of Natural Science and Technology, Okayama University, Setouchi, 701-4303, Japan
5 Department of Anatomy, Division of Histology and Cell Biology, Jichi Medical University, School of Medicine, Shimotsuke, 329-0498, Japan
6 Division of Ultrastructural Research, National Institute for Physiological Sciences, Okazaki, 444-8787, Japan
DOI:10.1016/j.isci.2020.101648
<研究について>
名古屋大学医学部・医学系研究科
糖尿病・内分泌内科学 教授 有馬 寛
<広報担当>
名古屋大学医学部・医学系研究科総務課総務係
自然科学研究機構 生理学研究所 研究力強化戦略室
自治医科大学大学事務部研究支援課
岡山大学総務・企画部広報課




名古屋大学医学部附属病院 糖尿病・内分泌内科
自然科学研究機構 生理学研究所
自治医科大学
岡山大学