Jee-Woong Kim, Seung Nam Park, Im Joo Rhyu (Korea Univ)
Tatsuo Arii, Keiji Imoto (NIPS)
The lobule of cerebellum is classified phylogenetically into archicerebellum, paleocerebellum and neocerebellum. The previous studies based on transmission electron microscopy reported the density of the synapses between parallel fiber varicosities and Purkinje cell dendritic spines is higher in neocerebellum than archicerebellum. The morphometric analysis of dendritic spines with high-voltage electron microscope was undertaken to reveal morphological diversity of the dendritic spine according to functional compartment of the cerebellum.
Adult rat cerebella were dissected and stained according to a rapid Golgi protocol. Four-micrometer sections were observed with high voltage electron microscopy and some morphometric analyses were performed with Scion Image. The density, length, diameters of spine neck, area of spine and spine shape distribution were measured in the lobule II, VI and X in the vermal and paravermal regions.
No significant differences in the density, length, and area of spine and spine shape distribution throughout the cerebellar lobules were observed. The diameters of dendritic spine neck showed moderate difference in the case of mushroom and branched-type spines. The diameters of dendritic spine in neocerebelum (VI) showed a tendency smaller than that of spine neck in the lobule II and X. The dendritic spine morphology of Purkinje cells did not show remarkable difference throughout the lobules.
We need to do more works to explain the different results in this study from the previous reports.
樋田一徳(徳島大学大学院ヘルスバイオサイエンス研究部形態情報医学分野)
有井達夫(自然科学研究機構生理学研究所脳機能計測センター形態情報解析室)
我々はこれまで嗅球のニューロンとグリア構成について超高圧電子顕微鏡による三次元構造解析を行ってき た。従来,免疫電子顕微鏡でシナプス結合を同定した介在ニューロン群の解析を進めたが,本実験では,嗅球への遠心性入力成分であるセロトニン(5- hydroxytryptamine; 5-HT)ニューロンの三次元構造について解析を行った。
5-HT含有ニューロンはラット及びマウス脳内では脳幹縫線核に起始し全脳に投射分布している。光学顕 微鏡による観察では,嗅球には5-HT免疫陽性の線維のみで細胞体はない。5-HT線維は,糸球体層に最も密に分布し,次いで顆粒細胞層に多いが外網状層 には線維は少なく,最表層の嗅神経層には観察されない。そこで本実験では,糸球体層の5-HT線維について解析を行った。
糸球体層では5-HT線維は,層を横断する像が共焦点レーザー顕微鏡にて観察される。しかし単一の5-HT線維を追跡するには限界があり,糸球体内での正確な分布,隣接の傍糸球体領域及び複数の糸球体間の連続性は不明である。
固定した嗅球から50mm厚のスライスを作製,抗5-HT抗体,ビオチン化二次抗体,ナノゴールド・蛍光(FITC or Alexa) 同時標識ストレプトアビジンによりレーザー顕微鏡で観察後,Co/Ni増感DAB及び銀増感を行い,更に2~5mm厚の切片を作製し,超高圧電子顕微鏡で立体観察を行った。
糸球体内で5-HT線維は偏在せず構造内全体に一部分枝をしながら蛇行し分布伸長している。頻繁に数珠 玉状構造を呈し,膨大部ではミトコンドリアが観察される。以前解析したtyrosine hydroxylaseニューロンほど密な分布ではなく,またcalbindinやcalretininニューロンのような蜂巣状構造は示さない。この 5-HT線維は糸球体内のみならず隣接する傍糸球体領域にも存在し,糸球体内線維と連続し,複数の糸球体を横断する像が観察された。
5-HT線維は投射ニューロン及び各種介在ニューロンと接触しシナプス結合を形成していることが観察さ れている。このため,本実験解析知見とも併せて,複数の糸球体での異種のニューロン群への遠心性調節効果が今後解明されるべき課題として提起される。現 在,シナプス結合を形成するニューロン種の定量的同定と,他の層を含めた超高圧電子顕微鏡を用いたより詳細な三次元構造解析を行っている。
野田 亨(藍野大学医療保健学部理学療法学科)
免疫組織化学的染色法は,現在,特定の蛋白分子を標識する方法として広く用いられている。この方法のう ち,比較的感度がよく,電子顕微鏡による観察に適した酵素抗体法を基本として,それに古典的な還元オスミウム溶液による染色法を組み合わせることによっ て,これまでの酵素抗体法で生じる反応産物の電子密度を超高圧電子顕微鏡による観察に耐えるほどに向上させ,細胞小器官等の立体構造観察を可能にしようと 試みた。4% パラホルムアルデヒドで固定したラットの組織をクリオスタットを用いて約10mm厚 の凍結切片とし,免疫組織化学に使用した。一次抗体としてはライソゾーム全体を標識させるためにライソゾーム酵素であるcathepsin Dに対する抗体,小胞体全体を標識させるために可溶性小胞体内のカルシウム結合蛋白であるcalreticulinに対する抗体等を一次抗体とし,それぞ れに蛍光標識を付けた二次抗体で反応性を確認した後,同条件の別の切片を用いて,酵素抗体法を行った。二次抗体を反応させた後に,DAB反応を行い,1つ のグループは通常の25mM PIPES緩衝1% 四酸化オスミウムで,もう1つのグループはこれまで知られている還元オスミウムを用いた染色法のうちZinc iodide osmium (ZIO) 液を用いて後固定を行い,脱水,切片の上から樹脂を入れたBEEMカプセルで覆い,重合させた。硬化後スライドガラス上の切片を樹脂ブロック側に回収し, ダイアモンドナイフで1mm,あるいはそれ以上の厚さの厚切り切片を作製し,生理学研究所の超高 圧電子顕微鏡(H-1250M) で切片の観察を行った。これまでのところ2種類の一次抗体のによる反応性の違いは明瞭に認められるものの,通常の1% 四酸化オスミウムで後固定したものと,Zinc iodide osmium (ZIO) 液で後固定したものとの間では反応産物の電子密度に明瞭な差を認めることはできなかった。これまでの報告ではZIO染色法を今回,切片で利用しているこ と,あるいは免疫組織化学で頻用されているパラフォルムアルデヒド単独固定でも染色可能であるかなど,いくつかの点はまだ再確認すべき点もあり,今回の研 究結果においてZIO染色が試料の電子密度増加に有効でなかった原因の検討事項として,試料側の条件も再検討される必要があると考えられた。
片桐 展子(弘前学院大学・看護学部)
片桐 康雄(弘前学院大学・看護学部)
有井 達夫(生理研超高圧電顕)
Onchidium sp. 軟体動物,腹足類)は,卵嚢内でveliger幼生期を経て成体に近い形態まで生長した後に孵化する。柄眼は産卵後8日目のveliger幼生に原基が形 成され,そのまま成体の眼となる(片桐ら1999)。加温オスミウム染色は組織に高いコントラストを与えるので,超高電圧電顕を用いると準厚切切片におい ても微細構造が,通常の電顕のように観察可能である。特に柄眼の光受容細胞内のphotic vesicles (PV) は加温オスミウム染色で黒染される(図1)。PVは軟体動物視細胞にあるロドプシンーレチノクロム系におけるレチノクロムの局在部位として知られる。 veliger幼生は小さく,眼の部位は固定試料では識別できない。準厚切連続切片を作成し,超高電圧電顕観察によって柄眼の形成過程を明らかにしたい。
【材料と方法】イソアワモチ類の産卵後10日目veliger幼生と孵化後の幼動物を2% オスミウム水溶液で40°,48時間処理,エポン包埋した。0.2~0.3mm厚さの連続切片を酢酸ウランと鉛染色,超高圧電顕で1,500~20,000倍で観察した。
【結果と考察】イソアワモチ類は多種類で多数の光受容器からなる特異な多重光受容系を持つ。柄眼は主要な光受容器で,直径200mm,球形の胞状で,角膜と網膜からなり,内部にレンズがある。網膜に2タイプの感杆型光受容細胞と支持細胞が区別される。黒い色素顆粒が網膜の細胞に含まれるが角膜細胞にはない。タイプ1の光受容細胞は微絨毛とPVsが特徴である。
10日目veliger幼生の眼は直径12mmと小さく,構成細胞も少ない。色素顆粒は含まれるが,微絨毛は未発達, PVsは認められない。支持細胞との識別ができない(図2A,B)。孵化後の幼動物は直径22mm,構成細胞は多くなり,小型であるが成体の眼に近い。微絨毛は光受容細胞の頂部からレンズを囲むように束状で存在,PVsは黒染せず,支持細胞との識別も難しい(図3A,B)。加温オスミウム染色によって粗面小胞体やゴルジ装置,核膜腔が黒染されている。
幼生と幼動物の眼は黒点として識別されるが,光受容細胞にPVsは明瞭に認められなかった。その理由として,①眼は形成途中にありPVsがまだ形成されていないか少量である,②PVsがまだ未成熟で,オスミウム染色に不染であることが考えられる。
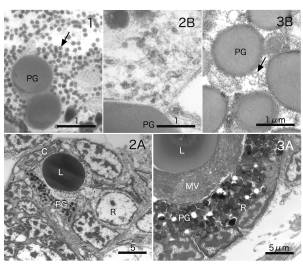
図1 成体の柄眼。タイプ1感桿型光受容細胞の細胞質内にあるphotic vesicle(↓)は黒染。
図2A, B 10日目veliger幼生の眼。網膜(R)の細胞に色素顆粒(PG) は含まれるが,微絨毛は未発達, PVsは認められない。
図3A, B 孵化後の幼動物の眼,網膜(R)の細胞に多数の色素顆粒(PG)が含まれる。微絨毛(MV)は束状にレンズ(L)を囲む。photic vesicle(↓)は黒染しない。
C;角膜の細胞
遠藤 泰久・吉村 亮一・西田 倫希(京都工芸繊維大学)
有井 達夫
神経細胞の突起の途中に形成される数珠状の膨大部(varicosity) はシナプス形成に関わるだけでなく,脳内や末梢組織における非シナプス的情報伝達部位として機能している。我々のこれまでの培養細胞を用いた研究によ り,varicosityの形成頻度が標的細胞との混合培養によって増加すること,anterogradeだけでなくretrogradeにも移動するこ と,微小管形成阻害剤taxolにより動きが抑制されることなどが明らかとなっている。しかし,その形成機構はほとんど不明のままであり,超高圧電子顕微 鏡により細胞骨格の微小管の3次元構造解析を試みた。
ホルムバール支持膜を張った金メッシュを70%エタノールで滅菌後,コラーゲンコートを施し,神経細胞株NG108細胞をDMEM培地に1mM dbcAMPを添加し3日間培養した。細胞を0.1%Triton X-100,0.1M PIPES,1mM MgSO4,2mM EGTA,2M glycerol,pH6.75で10-15分処理し,チュブリンのモノマーなど低分子を抽出後,4%パラフォルムアルデヒド固定した。抗チュブリン抗体 によりABC-HRP法で免疫染色し,DAB,硫酸ニッケルアンモニウムで発色した。1%オスミウム酸で後固定し,エタノール系列で脱水し,二酸化炭素− 臨界点乾燥を行った。試料をカーボン蒸着後,超高圧電子顕微鏡(H-1250M 加速電圧1,000kV)により,同一視野を-60度から+60度まで2 度刻みの傾斜連続写真を撮影し,IMODにより神経突起およびvaricosityにおける微小管の3次元画像解析を行った。
 |
 |
|
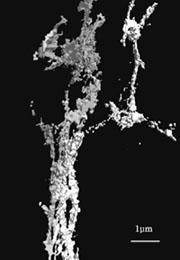
図1:NG108細胞の神経突起およびvaricosityの一部の超高圧電子顕微鏡写真。抗チュブリン抗体により微小管のコントラストを高めている。 |
図2:NG108細胞の神経突起およびvaricosityにおける微小管の3D image。 |
長浜真人(鈴鹿医療科学大学医用工学部)
有井達夫(生理学研究所形態情報解析室)
消化管壁内神経叢内には多くのニューロンが含まれておりその数は脊髄に含まれるニューロン数に相当しま す。これらの壁内ニューロンは形態学的にサブタイプに分類されていますが,細胞体周囲の複数の短い樹状突起と一本の長い軸索様突起を持つDogiel I型のニューロンは運動性ニューロンあるいは介在性ニューロンの性格を持ち,VIP,PACAP,5-HTなどの神経活性物質を含有することが知られてい ます。VIPは平滑筋に対し,弛緩作用を示す神経ペプチドで,VIPを含有するニューロンは筋層間神経叢内において抑制性運動ニューロンとして機能すると 考えられています。既に私共の報告でこれらの樹状突起様突起には多数のシナプス入力が確かめられておりましたが,微細な三次元構築に関する解析はありませ んでした。今回,我々は免疫染色(ABC法とニッケル・コバルト増感法)を施したVIP含有ニューロンをプラスチック包埋し,3-5ミクロン切片を作製し て超高圧電子顕微鏡にて観察しました。超高圧電顕により,①ニューロンの細胞体周囲に微細で短い突起を立体的に観察することができました。②入力する長い 軸索様突起と樹状突起様突起あるいは神経細胞体との三次元的な位置関係を観察することができました。今後,超薄切切片による通常電顕観察の連続切片による シナプス軸索様突起と樹状突起様突起のシナプス構築関係と今回の超高圧電顕所見を比較対照し,消化管ニューロンのシナプス伝達機構の解析を計画しておりま す。
【追加情報】(調査月2007年8月、記入月2008年6月)
関係論文
Emi Kiyokage, Yuzhen Pan, Adam C. Puche, Michael T. Shipley
(Department of Anatomy and Neurobiology, University of Maryland School of Medicine, MD, USA)
Kazunori Toida (Department of Anatomy and Cell Biology,
Institute of Health Biosciences, The University of Tokushima)
The olfactory bulb is specialized for the neural processing the molecular signals of smell. Mitral and tufted cells are projection neurons of the olfactory bulb. These neurons receive synaptic inputs from olfactory sensory neurons in the glomerui and project their axons into higher cortical structures. This pathway is regulated by inhibitory interneurons such as periglomerular cells, granule cells, and other kind of interneurons. We have been investigating the neuronal organization of the olfactory bulb by both structural and physiological analyses. To understand synaptic effects of GABAergic interneurons, we need to know the distribution and localization of GABA receptors in the olfactory bulb. We have started analyzing three-dimensional ultrastructures of physiologically identified neurons and the organization of GABA receptors in the olfactory bulb by high-voltage electron microscopy (HVEM).
All experiments were performed on olfactory bulb slices obtained from male GAD65 and TH transgenic mice expressing green fluorescent protein (GFP). TH-GFP (+) cells were recorded by whole cell patch clumping. After that biocytin filled cells were stained with Co/Ni-DAB and reconstructed by Neurolucida. In contrast, GAD6-GFP slices were double immunostained with anti-GFP and anti-GABAA receptor antibodies and labeled by colloidal gold. All these slices were embedded in Epon-Araldite resin, resectioned at 1-3 mm using ultramicrotome, and examined with HVEM.
It was possible to observe three-dimensional structure of biocytin filled TH neurons using HVEM. GABAA receptors were mainly distributed along membrane of cell bodies, primary, and secondary dendrites of mitral cells and some receptors were found in the cytoplasm. In the glomerular layer, GABAA receptors were localized in glomerular neuropil, and cell bodies of GFP positive cells which existed in the periglomerular region. We are investigating optimal staining condition for suitable contrast to visualize TH neurons. We will investigate their type of cells expressing GABAA receptors on dendrites in the glomeruli. Our goal is to provide a quantitative analysis of GABAA receptor on several classes of olfactory bulb neurons.
Kim, InSun (Biology Department, Keimyung University)
The ultrastructure of plastids was investigated in succulent leaves of Sedum rotundifolium to examine changes that occur during leaf development. In the study, leaves were placed into etiolated, immature, young, and mature categories by developmental stage and size. Features of tubular inclusion bodies and starch grains in the plastids were of particular interest. The vacuole size, tubular inclusion bodies and starch grains in the plastids became remarkably different as the leaves developed. Etioplasts of the unexposed leaves had prolamellar bodies, abundant starch grains, large tubular inclusion bodies, few plastoglobuli, and thylakoid systems. Membranes of the thylakoids were still continuous with those of the prolamellar body. The plastids were often influenced by the presence and profile of inclusion bodies and starch grains throughout early stages. Morphology was highly variable in the etioplasts but consistently hemispherical or ovoid in mature chloroplasts. Tubular inclusion bodies were most abundant in the etiolated leaves, but disappeared completely with development. Starch grains were also significantly reduced in size. Young and mature mesophyll cells exhibited normal chloroplast ultrastructure and huge central vacuoles with extremely thin peripheral cytoplasm. Grana were extensive and comprised a large portion of the chloroplasts. Traces of peripheral reticulum were also discovered in chloroplasts of the expanded leaves. Implications of ultrastructural changes in tubular inclusions and starch grains during development are discussed with relevance to Crassulacean acid metabolism (CAM).
Seok-Won Jeong, Young R. Seo (Dep. Pharmacology, Institute for Basic Medical Science,
Medical Research Center, School of Medicine, Kyung Hee University)
Apoptosis-related signaling pathway has been recently highlighted due to the very important implications on numerous health problems including neurodegenerative disease. Bax inhibitor-1 (Bi-1) protein has been known to have ability to suppress Bax-induced apoptosis in mammal cells. Though the Bi-1 was reportedly suggested to play a role in endoplasmic reticulum (ER)-mediated stresses, the function and localization of the Bi-1 protein has not been clear. Our recent study using conventional electron microscopy, we confirmed the localization of Bi-1 associated with ER membrane. Furthermore, we also found the localization of Bi-1 in mitochondria as a novel aspect of Bi-1 for the role in apoptosis process. In this study, potential roles of Bi-1 protein in mitochondria-dependent apoptosis has been investigated employing a high voltage electron microscopy (HVEM), which has been effectively applied to study the three-dimensional structure. Particularly, we are focusing on the alteration of mitochondrial structure in human 293 cells, depending on Bi-1 functional status. Our ongoing study from the reconstructed images of the mitochondrial formation in Bi-1 normal and Bi-1 defective 293 cells might be able to give a new insight on understanding the process of programmed death in mammal cells.
Ji Young Mun, Kyung Eun Lee, Se Jin Park, Sung Sik HAN
(School of Life Sciences and Biotechnology, Korea University)
The Drosophila retinal cell is widely used to study development and cell signaling processes. In the past decades, conventional chemical fixation has been used to study the structure of retinal cells in Drosophila. Rapid freezing methods are superior to chemical fixation methods due to their fixation speed. Some Drosophila tissues, such as the eyes, do not freeze well due to their surrounding cuticle layer. Therefore, in the case of the Drosophila retina, the benefits of high pressure freezing and freeze substitution (HPF-FS) have not been fully realized. In this study, a retinal cell from Drosophila melanogaster was studied using the HPF-FS method. Compared to chemical fixation, the preservation of the cytoplasm in the HPF-FS sample was improved on the whole. The HPF-FS cell membranes were smoother than that of chemical fixation. In addition, HPF-FS preserved the mitochondria structures very well. These results of the present study suggest that HPF-FS is superior to other fixation methods for the preservation of the retinal cell structure.
濱 清(生理学研究所)
Ellisman, MH (NCMIR, UCSD)
ラット脳内神経細胞突起の三次元再構築にあたり,二軸傾斜で撮影された画像を処理することを進めている。
生理研で使用しているUCSD,NCMIRによるトモグラフィーソフトは,旧型で処理に時間がかかる。一方,コロラド大で開発されたIMODトモグラフィーソフトは,広く普及して自動化が進んでおり使用が容易で高速である。
このソフトでは,二軸傾斜による画像の解析ソフトを備えており,これによりトモグラフィー解析の信頼性 が向上することが期待される。二軸傾斜の条件を満たす状態で加速電圧1,000kVで±60度の範囲で2度おきに撮影された超高圧電子顕微鏡画像に応用し て解析を進めている。一軸傾斜で撮影されたそれぞれの断層像を融合したときに得られる画像の精度を検討し,応用の可能性を検討している。
小曽戸陽一,末次妙子(理化学研究所・発生再生科学総合研究センター)
樋田一徳,清蔭恵美(徳島大学大学院・神経情報医学部門・情報統合医学講座・形態情報医学分野)
有井達夫 (生理学研究所・脳機能計測センター・形態情報解析室)
中枢神経系神経細胞の前駆細胞である神経上皮細胞は,主にneuroepitheliumの apical表層で細胞分裂を行う。脳発生の初期には,細胞増殖のための対照的な分裂,後に神経細胞を生み出す非対称的分裂(一つの神経上皮細胞から,神 経上皮細胞および神経細胞が生成する)が一定の割合で見受けられる。近年のタイムラプス観察により,分裂期では細胞体とbasal laminaのコンタクトは大変細長い形状(直径1mm以下,長さ100mm以上)となるものの,プロセス様の構造物 (basal process)として保持されていることが示された。しかしながら,細胞分裂の際にbasal processがどのように娘細胞に引き継がれるかについては不明な点が多い。現在までの報告では,basal processはその極めて細長い構造上,細胞分裂の際には分裂することはなく,どちらかの娘細胞に不均等に分配されるとされている。その不均等な分配が娘細胞の非対称な運命決定(増殖的あるいは神経生成的)に働いているとの示唆もある。
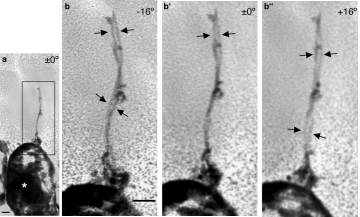
我々は,basal processの形態学的情報を得るためには電子顕微鏡観察が必要であると考え,これまでに様々な手法による観察を試みてきた。当初通常型の電子顕微鏡を用いてその観察を試みたが,細長いbasal processの全体構造を把握することは極めて困難であった。また,走査型電子顕微鏡による観察も行ったが,神経上皮組織のように混み合った状況では,basal processの形態を追うことがやはり困難であった。そこでこれら通常型電子顕微鏡の弱点を克服できる,すなわち厚い試料(5mmまで)の観察が可能である,生理学研究所の超高圧電子顕微鏡(H-1250M) によるbasal processの観察を,前年度に引き続き行った。我々はこれまでに,マウス10.5日胚の終脳の神経上皮細胞のbasal processの微細構造を評価するための観察手法の確立を行ってきた。それらのうち,ゴルジ染色法と超高圧電子顕微鏡を組み合わせることによりbasal processを可視化する方法がもっとも適していると考え,この方法で多くのサンプルを観察した(図1)。この観察の結果,細胞分裂期において,basal processがその非常に細長い構造にもかかわらず,細胞体分裂より前の段階で分裂している可能性を示す知見を得る事に成功した。
現在我々は,上記の超高圧電子顕微鏡の観察結果を含めた,神経上皮細胞のbasal processの細胞分裂時の挙動に関する知見をまとめた論文を投稿中である。
|
図1 |
細胞分裂期の哺乳類神経上皮細胞の超高圧電子顕微鏡像。 aは低倍率,b-b”は,aの黒四角部分の拡大像。b-b’,b’-b”は,それぞれステレオペア写真となっている。矢印は,対となる2本のbasal processが細胞体 (*) から伸長していることを示している。Bar=1mm |
日 高 聰(藤田保健衛生大学医学部生理学教室)
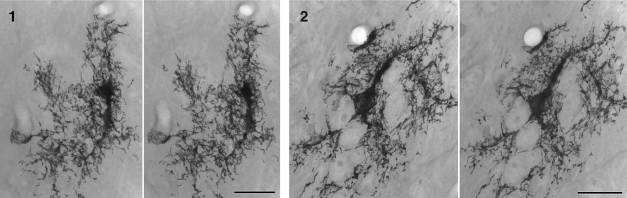
ニューロン間での電気シナプスの形成について,発現するコネクシンの型が解明され,実験手法を組み合わせた解析が可能になった。電気シナプスを電気生理学的に解析したニューロンを細胞内標識し,超薄切片でギャップ結合を同定すると共に,5mm の厚さの切片を1,000kVの加速電圧の超高圧電子顕微鏡下で解析することによって,電気シナプスを形成する樹状突起の立体構造を解明する。蛍光染色し たニューロンに,抗コネクシン抗体を用いた免疫細胞化学法を適用し,共焦点レーザースキャン顕微鏡で解析することによって,樹状突起間の電気シナプスの部 位を特定できるようになった。
視覚系のニューロンに注目して,視覚中枢に出力する網膜神経節細胞間や,網膜内三次の介在ニューロン・ 抑制性のアマクリン間の電気シナプスの機能構造解析を行なった。Dualpatch-clamp法によって通電実験を行い,電気シナプスの形成度を判断し た。二連の電圧固定法で細胞間電流を測定し,細胞間チャネルの最大コンダクタンスを測定した(網膜神経節細胞間2.45 nS,アマクリン細胞間5.48 nS)。細胞ペアをLuciferyellowで標識して解析した結果,樹状突起間の接触部位は平均7個(網膜神経節細胞間,n = 12),23個(アマクリン細胞間,n = 24)であった。一方,5mmの厚さの 切片を作成し,超高圧電子顕微鏡で樹状突起の立体構造を解析し,接触部位はclosemembraneappositionの形態を呈することが分かっ た。超薄切片で樹状突起間の接触部位に微細形態的なギャップ結合を同定した。超高圧電子顕微鏡の解析標本 で,closemembraneapposition形態の接触領域を計測することによって,ギャップ結合斑の大きさを測定した。平均直径は,網膜神経節 細胞間で0.86mm (n = 14) アマクリン細胞間で7mm (n = 24)(図1)であった。そこで,ギャップ結合の開口チャネルの割合を見積もった。凍結割断レプリカ法で得られたギャップ結合斑のコネクソン粒子の形態と 密度(図2),細胞間でのギャップ結合の存在数と,報告されている最大シングルチャネルコンダクタンスから,コネキシンチャネルの開口確率が均一でないと 仮定した場合,測定した最大細胞間チャネルコンダクタンスから,ギャップ結合の開口チャネルの割合は,網膜神経節細胞間で0.8%,アマクリン細胞間で 0.2%と計算された。網膜ニューロン群が同期して活動電位を発生していることを考えた場合に,このチャネル開口率の妥当性を検討した。
文献
1) Hidaka, S. et al., (2004) Journal of Neuroscience,24 (46): 10553-10567.
2)Hidaka, S. et al. (2005) Journal of Integrative Neuroscience, 4 (3): 313-340.
3) 日 高 聡 (2006)日本顕微鏡学会誌「顕微鏡」41 (2): 117-119.

|

|
【追加情報】(調査月2007年8月、記入月2008年6月)
発表論文
小澤一史(日本医科大学 大学院医学研究科 生体制御形態科学分野)
生体は絶えず変化する外的環境に対応するよう,体内の生理的状態を恒常的に保とうとする機構,すなわちホメオスターシス homeostasisを有している。このホメオスターシスにひずみを生じさせる物理的,精神的事象がストレス stressである。興味深いことに,物理的,精神的事象のいずれにしても,ストレスは下垂体前葉からのACTH(adreno- corticotropic hormone 副腎皮質刺激ホルモン)分泌を促し,副腎皮質からコルチゾール cortisolを分泌させる。したがって,血中のコルチゾール値の量を見ることによって,ストレスを受けているかどうかを判断することが出来る。
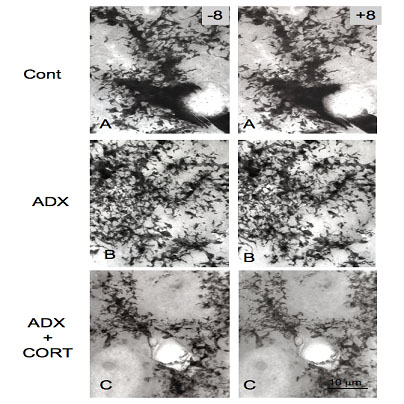
海馬は,この副腎皮質ホルモンであるコルチゾールの受容体を有する神経細胞やグリア細胞(特に星状グリ ア細胞)が多数発現しており,脳におけるストレス応答の中核中枢として反応する部位であり,これまでに特に神経細胞における微細構造の変動について,報告 がなされてきた。一方,グリア細胞の形態変化については,あまりはっきりとした報告はない。そこで,コントロール(対照)群,副腎摘出 (ADX) 群,副腎摘出+コルチコステロン (CORT) 補充群の3群におけるグリア細胞の形態変化について,ゴルジ染色を施したラット脳の標本を用いて,超高圧電子顕微鏡観察を行った。コントロール群に比 べ,ADX群では,顕著なグリア細胞の数の増加とともに微細形態的に細胞の肥大と突起の拡がりが認められ,CORTの補充により,コントロール群に近い形 状に戻る様子を示した。
これらの変化は,同じ実験環境における神経細胞の形態変化と逆の現象の傾向を示しており,神経細胞の機能形態と連動するグリア細胞の機能変化を示唆し,興味深い所見であると考えられ,現在,さらに多角的な検索を進めている。
 |
|
図の説明:超高圧電顕で観察する星状グリア細胞のステレオ像 (A)コントロール群、(B) 副腎摘出(ADX)群、(C) 副腎摘出+コルチコステロン補充 (ADX+CORT) 群。ADX群において、グリア細胞の顕著な肥大、突起の拡張が観察される。Bar = 10 mm |
発表論文
学会報告